
| A. | 用水可以鉴别乙醇、苯、和溴苯 | |
| B. | 甲苯与氯气在光照下可发生取代反应,主要生成2,4-二氯甲苯 | |
| C. | 化学式为C7H16的有机物,分子中含有3个甲基的可能结构有3种 | |
| D. | 乙酸丁酯中含乙酸杂质,可以加入饱和碳酸钠溶液洗涤,然后通过分液来去除杂质 |
分析 A.乙醇溶于水,苯和溴苯不溶于水,但二者密度大小与水不同;
B.甲苯与氯气在光照下可发生取代反应,取代甲基的氢原子;
C.分子式为C7H16的烃属于烷烃,含有3个甲基,则该烷烃只有1个支链;
D.乙酸丁酯不溶于饱和碳酸钠溶液,乙酸可与碳酸钠反应.
解答 解:A.乙醇溶于水,苯和溴苯不溶于水,苯的密度比水小,溴苯的密度比水大,可鉴别,故A正确;
B.甲苯在不同的条件下发生不同的取代反应,与氯气在光照下可发生取代反应,取代甲基的氢原子,如在催化作用下,取代苯环上的氢原子,故B错误;
C.3个甲基需要一个支链是甲基,主链是己烷,左右各有一个-CH3,支链的甲基只能加在2或3号C上,4号C与3号C相同,5号C与2号C相同,还有一种是含有乙基的,即3-乙基戊烷,共三种,分别是2-甲基己烷、3-甲基己烷与3-乙基戊烷,故C正确;
D.乙酸丁酯不溶于饱和碳酸钠溶液,乙酸可与碳酸钠反应,可用于除杂,故D正确.
故选B.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构特点以及官能团的性质,本题易错点为C,注意把握同分异构体的判断,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 澄清透明的溶液中:MnO4-、SO42-、K+、Fe3+ | |
| B. | 0.1 mol•L-1FeCl3溶液中:Mg2+、NH4+、SCN-、SO42- | |
| C. | 滴入甲基橙显黄色的溶液中:Na+、ClO-、I-、SO42- | |
| D. | 水电离产生的c(H+)=10-12 mol•L-1的溶液中:K+、Na+、NO3-、CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该混盐水溶液呈碱性 | |
| B. | 该混盐与H2SO4反应有气体生成 | |
| C. | 该混盐溶液加入BaCl2可以生成白色沉淀 | |
| D. | 该混盐在酸性条件下可生成S,每产生32g S转移2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 装置图 | 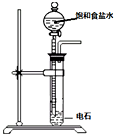 | 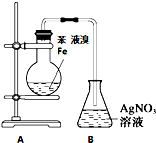 | 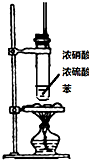 | 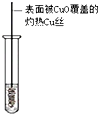 |
| 实验目的 | 乙炔的制备 | AgNO3验证苯与液溴发生取代反应 | 制备硝基苯 | 验证乙醇的还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
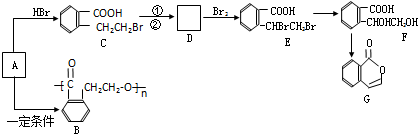
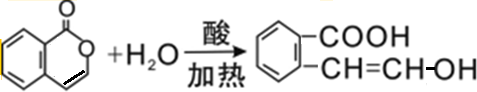
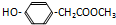 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
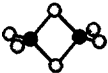 硼的最简单氢化物--乙硼烷球棍模型如图,由它制取硼氢化锂的反应为:2LiH+B2H6=2LiBH4
硼的最简单氢化物--乙硼烷球棍模型如图,由它制取硼氢化锂的反应为:2LiH+B2H6=2LiBH4查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
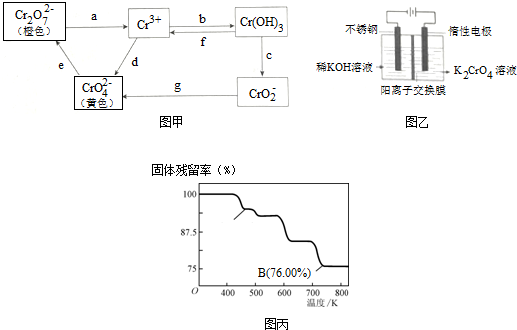
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com