
 实验室用乙酸和正丁醇制备乙酸正丁酯.CH3COOH+CH3CH3CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O有关物质的相关数据如下表.
实验室用乙酸和正丁醇制备乙酸正丁酯.CH3COOH+CH3CH3CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O有关物质的相关数据如下表.| 化合物 | 相对分子质量 | 密度g.cm-3 | 沸点/ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
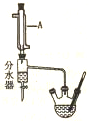
分析 I.(1)由仪器的结构可知a为冷凝管;
(2)有机物易挥发,有机反应复杂,温度过高时,挥发而损失,且副反应增加;
(3)分离出生成的水,有利于平衡向生成乙酸正丁酯的方向移动;
分水器中的水层量不再增加,说明反应结束;
Ⅱ.(1)饱和Na2CO3溶液可溶解正丁醇,中和酸,从而除去产品中的杂质;
(2)有机层的密度小于水,在上层,应从分液漏斗上口倒入蒸馏烧瓶中,再进行蒸馏;
(3)蒸馏获得乙酸正丁酯,由物质的沸点可知控制温度;
Ⅲ.先根据反应方程式计算酸和醇哪个过量,按照量少的计算理论上酯的量,再由实际上酯的量与理论值之比即为酯的产率.
解答 解:I.(1)由仪器的结构可知a为冷凝管,故答案为:冷凝管;
(2)温度过高时,正丁醇、乙酸易挥发,且副反应增加,导致酯产率降低,
故答案为:温度过高时,正丁醇、乙酸易挥发,且副反应增加,导致酯产率降低;
(3)反应生成酯与水,属于可逆反应,使用分水器分离出水,使平衡正向移动,提高反应产率;分水器中的水层量不再增加,说明反应到达终点,
故答案为:使用分水器分离出水,使平衡正向移动,提高反应产率;分水器中的水层量不再增加;
Ⅱ.(1)得到酯中含有挥发出的乙酸、正丁醇,饱和Na2CO3溶液可溶解正丁醇,中和酸,从而除去产品中的杂质,
故答案为:饱和Na2CO3溶液可溶解正丁醇,中和酸,从而除去产品中的杂质;
(2)有机层的密度小于水,在上层,分液完成后,有机层从分液漏斗上口倒入一个干燥的蒸馏烧瓶中,再进行蒸馏,
故答案为:有机层从分液漏斗上口倒入一个干燥的蒸馏烧瓶中;
(3)蒸馏获得乙酸正丁酯,由物质的沸点可知控制温度为126.1℃,
故答案为:126.1℃;
Ⅲ.18.5mL正丁醇的质量为18.5mL×0.80g/mL=14.8g,15.4mL冰醋酸的质量为15.4mL×1.045g/mL=16.093g,
设理论上14.8g正丁醇完全反应需乙酸的质量是y,则:
CH3COOH+CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
60g 74g
y 14.8g
y=$\frac{60g×14.8g}{74g}$=12g<16.093g,所以乙酸过量,按照正丁醇计算乙酸正丁醇酯的理论质量,
设乙酸正丁醇酯的理论质量为x,则:
CH3COOH+CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
74g 116g
14.8g x
所以x=$\frac{14.8g×116g}{74g}$=23.2g
则乙酸正丁酯的产率为 $\frac{12.76g}{23.2g}$×100%=55%,
故答案为:55%.
点评 本题考查有机物物质制备的实验,涉及化学仪器、对反应原理的理解应用、对操作的分析评价、物质的分离提纯、产率计算等,注意根据乙酸乙酯的制备进行知识迁移应用,较好的考查学生的分析能力、数据处理能力,难度中等.


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
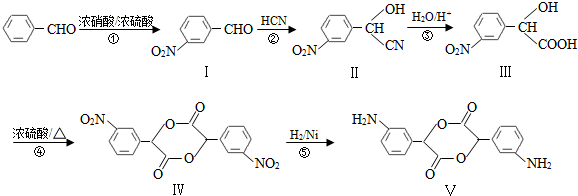
 ,和
,和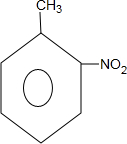 .
.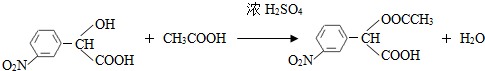 (要求写出反应条件),
(要求写出反应条件),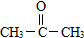 )代替化合物 I发生反应②可以得到化合物Ⅵ,化合物Ⅵ的结构简式为
)代替化合物 I发生反应②可以得到化合物Ⅵ,化合物Ⅵ的结构简式为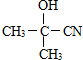 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
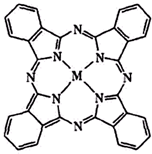 锂亚硫酰氯(Li-SOCl2)电池具有能量密度高、工作电压和放电电压平稳、工作温度范围宽及贮存寿命长等优点,在航海、医疗及井下油田设备等方面的应用广泛.
锂亚硫酰氯(Li-SOCl2)电池具有能量密度高、工作电压和放电电压平稳、工作温度范围宽及贮存寿命长等优点,在航海、医疗及井下油田设备等方面的应用广泛.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
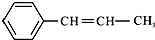 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 不溶于水,易溶于有机溶剂 | |
| B. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 | |
| C. | 能发生聚合反应,其产物可表示为: | |
| D. | 能使溴水褪色,但不能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
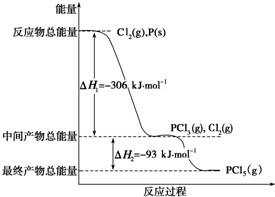 已知红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g),反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).
已知红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g),反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com