
| A. | 称取5.1gNa2CO3,加入500mL水 | |
| B. | 称取13.7gNa2CO3•10H2O,配成500mL溶液 | |
| C. | 称取5.3Na2CO3,加入500mL水 | |
| D. | 称取14.3gNa2CO3•10H2O,配成500mL溶液 |
分析 实验室里需用480mL 0.1mol•L-1的碳酸钠溶液,实际上配制的是500mL 0.1mol/L的碳酸钠溶液,需要碳酸钠的物质的量为:0.1mol/L×0.5L=0.05mol,需要碳酸钠的质量为:106g/mol×0.05mol=5.3g,若用Na2CO3•10H2O配制,需要Na2CO3•10H2O的质量为:286g/mol×0.05mol=14.3g,据此进行解答.
解答 解:实验室里需用480mL 0.1mol•L-1的碳酸钠溶液,实际上配制的是500mL 0.1mol/L的碳酸钠溶液,需要碳酸钠的物质的量为:0.1mol/L×0.5L=0.05mol,需要碳酸钠的质量为:106g/mol×0.05mol=5.3g,若用Na2CO3•10H2O配制,需要Na2CO3•10H2O的质量为:286g/mol×0.05mol=14.3g,
A.需要碳酸钠的质量为5.3g,且加入水的体积不是500mL,故A错误;
B.需要Na2CO3•10H2O的质量为:286g/mol×0.05mol=14.3g,故B错误;
C.不是加入500mL水,应该是配成500mL溶液,故C错误;
D.称取14.3gNa2CO3•10H2O,配成500mL溶液,所得溶液浓度为0.1mol/L,该操作方法合理,故D正确;
故选D.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确配制一定物质的量浓度的溶液方法为解答关键,注意A、C为易错点,注意加入水的体积与溶液体积的关系,试题培养了学生的化学实验、化学计算能力.


科目:高中化学 来源: 题型:实验题
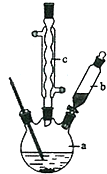 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线: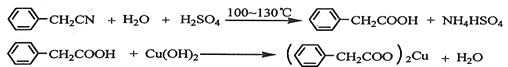
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①④⑤ | C. | ②③④ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 它的一氯代物只有一种同分异构体 | |
| B. | 它的二氯代物有两种同分异构体 | |
| C. | 它的分子式为C8H8 | |
| D. | 它与苯乙烯(C6H5-CH=CH2)互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2p1>p2 | B. | PCl5的分解率增大 | ||
| C. | p1>p2 | D. | Cl2的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,平衡时若充入稀有气体,SO2的转化率增大 | |
| B. | 0~6 min的平衡反应速率:v(O2)=0.105 mol/(L•min) | |
| C. | 保持其他条件不变,仅降低温度,正反应速率减小程度比逆反应速率减小程度大 | |
| D. | 反应开始时,向容器中通入的SO2的物质的量是1.4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
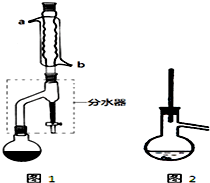 有机物的反应往往伴随副反应发生,因此 需要分离提纯.有一种水果香精的合成步骤如下:
有机物的反应往往伴随副反应发生,因此 需要分离提纯.有一种水果香精的合成步骤如下:| 化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
| 密度/(g/mL) | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点/℃ | 117.8 | 118.1 | 126.1 | 143 |
| 在水中的溶解性 | 易溶 | 易溶 | 难溶 | 难溶 |
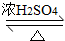 CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com