
【题目】(双选)将20mLNO2和NH3的混合气体,在一定条件下充分反应,化学方程式是:6NO2+8NH3![]() 7N2+12H2O。已知参加反应的NO2比NH3少2mL(气体体积均在相同状况下测定),则原混合气体中NO2和NH3的物质的量之比是
7N2+12H2O。已知参加反应的NO2比NH3少2mL(气体体积均在相同状况下测定),则原混合气体中NO2和NH3的物质的量之比是
A. 3∶2 B. 2∶3 C. 3∶7 D. 3∶4
科目:高中化学 来源: 题型:
【题目】有关天然产物水解叙述不正确的是
A、油脂水解可得丙三醇
B.可用碘检验淀粉是否水解完全
C、蛋白质水解的最终产物均为氨基酸
D.纤维素水解和淀粉水解得到的最终产物不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铝在生产生活中有广泛用途。
(1)铝元素位于元素周期表中第_______周期、第________族。
(2)19Al 是铝的一种核素,其中子数是_______。
(3)铝热反应可用于焊接钢轨,下图为铝热反应的实验装置图。
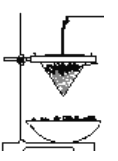
①该铝热反应的化学方程式是_______,该反应的现象是_______,此现象说明反应物的总能量_______生成物的总能量( 填“﹤ ” “﹥ ”“=”)。
②反应结束后,从沙中取出生成的固体物质,有同学推测该固体是铁铝合金,他设计了如下实验证明此固体中含有金属铝:取少量固体于试管中,滴加_______,当观察到_______现象时, 证明固体中含有金属铝。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是利用微生物燃料电池处理工业含酚废水的原理示意图,下列说法不正确的是
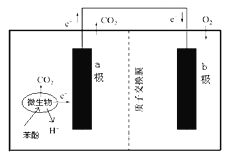
A.该装置可将化学能转化为电能
B.溶液中H+由a极移向b极
C.电极b 附近的pH降低
D.电极a附近发生的反应是C6H6O-28e- + 11H2O![]() 6CO2 + 28H+
6CO2 + 28H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全世界每年钢铁因锈蚀造成大量的损失。某城市拟用如图方法保护埋在酸性土壤中的钢质管道,使其免受腐蚀。关于此方法,下列说法不正确的是( )
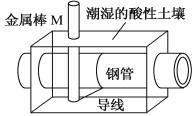
A.土壤中的钢铁易被腐蚀是因为在潮湿的土壤中形成了原电池
B.金属棒M的材料应该是比镁活泼的金属
C.金属棒M上发生反应:M-ne-=Mn+
D.这种方法称为牺牲阳极的阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1L0.1molL-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3H2O的变化趋势如右图所示(不考虑体积变化和氨的挥发),下列说法正确的是
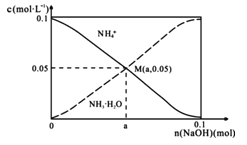
A.M点溶液中水的电离程度比原溶液大
B.在M点时,n(OH-)-n(H+)=(a -0.05)mol
C.随着NaOH的加入,![]() 不断增大
不断增大
D.当n(NaOH)=0.05mol时溶液中有: c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化铈(CeO2)是一种主要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2以及其他少量可溶于稀酸的物质)。某课题组就此粉末为原料回收铈,设计实验流程如下:
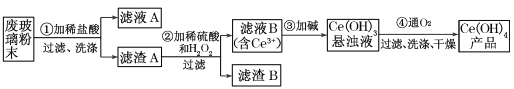
(1)洗涤滤渣A的目的是为了除去_____________(填离子符号),检验该离子是否洗净的方法是________________。
(2)第②步反应的离子方程式是___________________,滤渣B的主要成分是___________。
(3)萃取是分离稀士元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP_______(填“能”或“不能”)与水互溶。实验室进行萃取操作时用到的主要玻璃仪器有___________、烧杯、玻璃棒、量筒等。
(4)取上述流程中得到的Ce(OH)4产品0.536 g,加硫酸溶解后,用0.1000 mol·L-1FeSO4标准溶液滴定至终点时(铈被还原为Ce3+),消耗25.00 mL标准维液,该产品中Ce(OH)4的质量分数为_______________(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究NH3的性质具有重要意义。请回答下列问题:
(1)已知:①NH3 (g)+3O2(g)=2N2(g)+6H2O(g) △H=-1266.5kJ·mol-1
②N2(g)+O2(g)=2NO(g) △H=+180.5 kJ·mol-1
写出氨高温催化氧化生成NO的热化学方程式___________。
(2)氨气、空气可以构成燃料电池,其电池反应原理为:4NH3+302=2N2+6H2O。已知电解质溶液为KOH溶液,则负极的电极反应式为________。
(3)合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的化学平衡常数K值和温度的关系如下:

由上表数据可知该反应的△H_______ 0 填“> ”、“< ”或“=”) ;
理论上,为了增大平衡时H2的转化率,可采取的措施是_______(选填字母);
A.增大压强 B.使用合适的催化剂 C.升高温度 D.及时分离出产物中的NH3
③400℃时,测得某时刻氨气、氮气、氢气的物质的量浓度分别为3mol·L-1、2 mol·L-1、l mol·L-1,此时刻该反应的V正(N2)=______ V逆(N2)。(填“>”、“<”或“=”)。
(4)已知25℃时,Ksp[Fe(OH)3]=1.0×l0-38, Ksp[Al(OH)3]=3.0×l0-34,当溶液中的金属离子浓度小于1.0×10-5mol·L-1时,可以认为沉淀完全。在含Fe3+、A13+的浓度均为1. 05mol·L-1的溶液中加入氨水,当Fe3+完全沉淀时,A13+沉淀的百分数____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com