
ĻĀĮŠµ„ÖŹ»ņ»ÆŗĻĪļŠŌÖŹµÄĆčŹöÕżČ·µÄŹĒ
A£®Ź³Ę·°ü×°ÖŠ³£·ÅČėÓŠ¹č½ŗŗĶĢś·ŪµÄŠ”“ü£¬·ĄÖ¹Ź³ĪļŹÜ³±ŗĶŃõ»Æ±äÖŹ
B£®Na2O”¢Na2O2×é³ÉŌŖĖŲĻąĶ¬£¬ÓėCO2·“Ó¦²śĪļŅ²ĻąĶ¬
C£®SiO2ÓėĖį”¢¼ī¾łÄÜ·“Ó¦£¬ŹōÓŚĮ½ŠŌŃõ»ÆĪļ
D£®ŠĀÖĘĀČĖ®ĻŌĖįŠŌ£¬ĻņĘäÖŠµĪ¼ÓÉŁĮæ×ĻÉ«ŹÆČļŹŌŅŗ£¬³ä·ÖÕńµ“ŗóČÜŅŗ³ŹŗģÉ«

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗÓ±±Ź”øßČżÉĻѧʌŅ»µ÷æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A£®ĻņNa2CO3ČÜŅŗÖŠÖšµĪ¼ÓČėHCl£¬Ö±µ½²»ŌŁÉś³ÉCO2ĘųĢåĪŖÖ¹£¬ŌŚ“Ė¹ż³ĢÖŠ£®ČÜŅŗÖŠµÄHCO3-ÅØ¶Č±ä»ÆŹĒĻȱä“óŗó±äŠ”£ØČÜŅŗĢå»ż±ä»Æ¾łŗöĀŌ²»¼Ę£©
B£®ĻņNaHCO3ČÜŅŗÖŠ¼ÓČėBa(OH)2¹ĢĢ壬CO32-µÄÅØ¶Č±ä»ÆŹĒĻȱä“óŗó±äŠ”£ØČÜŅŗĢå»ż±ä»Æ¾łŗöĀŌ²»¼Ę£©
C£®ÓŠŗ¬0.2molNa2CO3ŗĶŗ¬0.3molHClµÄĮ½ÖÖČÜŅŗ£ŗ¢Ł½«Na2CO3ČÜŅŗÖšµĪµĪČėHClČÜŅŗÖŠ£»¢Ś½«HClČÜŅŗÖšµĪµĪČėNa2CO3ČÜŅŗÖŠ£¬¢Ł¢ŚĮ½ÖÖ²Ł×÷Éś³ÉµÄCO2Ģå»żÖ®±ČĪŖ3£ŗ2
D£®½«µČÖŹĮæµÄNa2OŗĶNa2O2ѳʷ·Ö±š·ÅČėµČĮæµÄĖ®ÖŠ£¬ĖłµĆČÜŅŗµÄÖŹĮæ·ÖŹż·Ö±šĪŖa%ŗĶb%£¬Ōņa”¢bµÄ¹ŲĻµŹĒa=b
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗž±±Ź”ĖÉ×ĢŹŠøßČżÉĻѧʌ9ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
½«Ņ»¶ØÖŹĮæµÄĆ¾ĀĮŗĻ½šĶ¶Čė100 mLŅ»¶ØÅØ¶ČµÄŃĪĖįÖŠ£¬ŗĻ½šĶźČ«Čܽā”£ĻņĖłµĆČÜŅŗÖŠµĪ¼ÓÅضČĪŖ5 mol/LµÄNaOHČÜŅŗ£¬Éś³ÉµÄ³Įµķøś¼ÓČėµÄNaOHČÜŅŗµÄĢå»ż¹ŲĻµČēĶ¼”££Øŗį×ų±źĢå»żµ„Ī»ŹĒmL£¬×Ż×ų±źÖŹĮ浄Ī»ŹĒg£©Ēó£ŗ
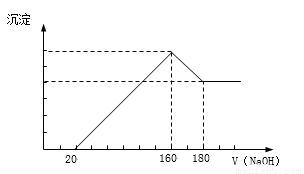
£Ø1£©¼ÓČėNaOHČÜŅŗ0--20mL¹ż³ĢÖŠ·“Ó¦·½³ĢŹ½ĪŖ£ŗ_______________”£160--180mL¹ż³ĢÖŠ·“Ó¦·½³ĢŹ½ĪŖ___________________”£
£Ø2£©ŗĻ½šÖŠMgµÄÖŹĮæĪŖ____________g”£ĖłÓĆHClµÄĪļÖŹµÄĮæÅضČĪŖ____________mol/L”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗž±±Ź”ĖÉ×ĢŹŠøßČżÉĻѧʌ9ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ¹ŲÓŚĢ¼Ēā»ÆŗĻĪļµÄĖµ·ØÕżČ·µÄŹĒ( )
A£®Ģ¼Ēā»ÆŗĻĪļµÄĶØŹ½ĪŖCnH2n+2
B£®Č¼ÉÕ²śĪļĪŖCO2ŗĶH2OµÄ»ÆŗĻĪļŅ»¶ØŹĒĢ¼Ēā»ÆŗĻĪļ
C£®Ģ¼Ō×Ó¼äŅŌµ„¼üĻąĮ¬µÄĢžŹĒĶéĢž
D£®ĶéĢž·Ö×ÓµÄĻą¶Ō·Ö×ÓÖŹĮæŅ»¶ØŹĒżŹż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗž±±Ź”ĖÉ×ĢŹŠøßČżÉĻѧʌ9ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
25”ę£¬Į½ÖÖĖįµÄµēĄė³£ŹżČēĻĀ±ķ”£
Ka1 | Ka2 | |
H2A | 1.3”Į10-2 | 6.3”Į10-6 |
H2B | 4.2”Į10-7 | 5.6”Į10-7 |
ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ
A£®H2AµÄµēĄė·½³ĢŹ½£ŗH2A=2H++A2-
B£®³£ĪĀĻĀ£¬ŌŚĖ®ÖŠNa2BµÄĖ®½āĘ½ŗā³£ŹżĪŖ£ŗ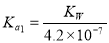
C£®µČÅØ¶ČµÄNa2AŗĶNa2BČÜŅŗ£¬ÓÉĖ®µēĄė²śÉśµÄH+ÅØ¶Č“óŠ”¹ŲĻµĪŖ£ŗĒ°Õß“óÓŚŗóÕß
D£®ĻņNa2BČÜŅŗÖŠ¼ÓČėÉŁĮæH2AČÜŅŗ£¬æÉ·¢Éś·“Ó¦£ŗB2-+H2A=A2-+H2B
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗŚĮś½Ź”“óĒģŹŠøßČżÉĻѧʌµŚŅ»“ĪÄ£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
Ó¦¶ŌĪķö²ĪŪČ¾”¢øÄÉĘæÕĘųÖŹĮæŠčŅŖ“Ó¶ą·½ĆęČėŹÖ”£
I£®ŃŠ¾æ·¢ĻÖ£¬NOxŹĒĪķö²µÄÖ÷ŅŖ³É·ÖÖ®Ņ»£¬NOxÖ÷ŅŖĄ“Ō“ÓŚĘū³µĪ²Ęų”£
ŅŃÖŖ£ŗN2(g)+O2(g) 2NO(g) ”÷H=+180.50kJ”¤mol£1
2NO(g) ”÷H=+180.50kJ”¤mol£1
2CO(g)+O2(g) 2CO2(g) ”÷H=£566.00 kJ”¤mol£1
2CO2(g) ”÷H=£566.00 kJ”¤mol£1
ĪŖĮĖ¼õĒį“óĘųĪŪČ¾£¬ČĖĆĒĢį³öŌŚĘū³µĪ²ĘųÅÅĘų¹ÜæŚ²ÉÓĆ“ß»Æ¼Į½«NOŗĶCO×Ŗ»Æ³ÉĪŽĪŪČ¾ĘųĢå²ĪÓė“óĘųŃ»·£¬Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ ”£
II£®æŖ·¢ĄūÓĆĒå½ąÄÜŌ“æɼõÉŁĪŪČ¾£¬½ā¾öĪķö²ĪŹĢā”£¼×“¼ŹĒŅ»ÖÖæÉŌŁÉśµÄĒå½ąÄÜŌ“£¬¾ßÓŠ¹ćĄ«µÄæŖ·¢ŗĶÓ¦ÓĆĒ°¾°£¬Ņ»¶ØĢõ¼žĻĀÓĆCOŗĶH2ŗĻ³ÉCH3OH£ŗCO(g)+2H2(g) CH3OH(g)£¬ŌŚ2LĆܱÕČŻĘ÷ÖŠ³äČėĪļÖŹµÄĮæÖ®±ČĪŖ1:2µÄCOŗĶH2£¬ŌŚ“߻ƼĮ×÷ÓĆĻĀ³ä·Ö·“Ó¦”£Ę½ŗā»ģŗĻĪļÖŠCH3OHµÄĢå»ż·ÖŹżŌŚ²»Ķ¬Ń¹ĒæĻĀĖęĪĀ¶ČµÄ±ä»ÆČēĻĀĶ¼ĖłŹ¾”£
CH3OH(g)£¬ŌŚ2LĆܱÕČŻĘ÷ÖŠ³äČėĪļÖŹµÄĮæÖ®±ČĪŖ1:2µÄCOŗĶH2£¬ŌŚ“߻ƼĮ×÷ÓĆĻĀ³ä·Ö·“Ó¦”£Ę½ŗā»ģŗĻĪļÖŠCH3OHµÄĢå»ż·ÖŹżŌŚ²»Ķ¬Ń¹ĒæĻĀĖęĪĀ¶ČµÄ±ä»ÆČēĻĀĶ¼ĖłŹ¾”£
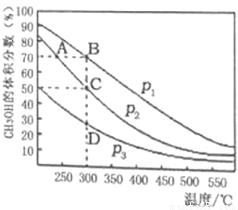
£Ø1£©øĆ·“Ó¦µÄ·“Ó¦ČČ”÷H 0£ØĢī”°£¾”±»ņ”°£¼”±£©£¬Ń¹ĒæµÄĻą¶Ō“óŠ”ÓėP1 P2£ØĢī”°£¾”±»ņ”°£¼”±£©”£
£Ø2£©øĆ·“Ó¦»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½ĪŖ ”£
£Ø3£©ĻĀĮŠø÷ĻīÖŠ£¬²»ÄÜĖµĆ÷øĆ·“Ó¦ŅŃ¾“ļµ½Ę½ŗāµÄŹĒ ”£
A£®ČŻĘ÷ÄŚĘųĢåŃ¹Ēæ²»ŌŁ±ä»Æ
B£®v(CO)£ŗv(H2)£ŗv(CH3OH)=1:2:1
C£®ČŻĘ÷ÄŚµÄĆÜ¶Č²»ŌŁ±ä»Æ
D£®ČŻĘ÷ÄŚ»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»ŌŁ±ä»Æ
E£®ČŻĘ÷ÄŚø÷×é·ÖµÄÖŹĮæ·ÖŹż²»ŌŁ±ä»Æ
£Ø4£©Ä³ĪĀ¶ČĻĀ£¬ŌŚ±£Ö¤H2ÅØ¶Č²»±äµÄĒéæöĻĀ£¬Ōö“óČŻĘ÷µÄĢå»ż£¬Ę½ŗā £ØĢī×ÖÄø£©”£
A£®ĻņÕż·“Ó¦·½ĻņŅĘ¶Æ B£®ĻņÄę·“Ó¦·½ĻņŅĘ¶Æ C£®²»ŅʶÆ
×÷³ö“ĖÅŠ¶ĻµÄŅĄ¾ŻŹĒ ”£
III£®ŅĄ¾ŻČ¼ÉÕ·“Ó¦ŌĄķ£¬ŗĻ³ÉµÄ¼×“¼æÉŅŌÉč¼ĘČēĶ¼ĖłŹ¾µÄČ¼ĮĻµē³Ų×°ÖĆ”£
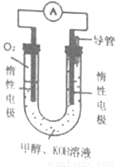
£Ø1£©øŗ¼«µē¼«·“Ó¦Ź½ĪŖ ”£
£Ø2£©µē³Ų¹¤×÷Ź±£¬ČōµēĮ÷Ēæ¶ČĪŖI£¬1øöµē×ÓĖł“ųµēĮæĪŖq£¬NAĪŖ°¢·üŁ¤µĀĀŽ³£ŹżµÄÖµ£¬ŌņøĆ×°ÖĆĆæ·ÖÖÓĻūŗļד¼µÄĪļÖŹµÄĮæĪŖ mol£Ø¼ŁÉč»ÆѧÄÜČ«²æ×Ŗ»ÆĪŖµēÄÜ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗŚĮś½Ź”“óĒģŹŠøßČżÉĻѧʌµŚŅ»“ĪÄ£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÄĻŗ£Õł¶Ė”¢ÄĻŗ£ÖŁ²Ć°øŅ»Ö±Ē£¶Æ¹śČĖµÄŠÄ£¬ÄĻŗ£ŹĒŅ»øö¾Ž“óµÄ׏Ō“±¦æā£¬ŗ£Ė®æŖ·¢ĄūÓĆµÄ²æ·Ö¹ż³ĢČēĻĀĶ¼ĖłŹ¾”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ£Ø £©

A£®µŚ¢Ł²½ÖŠ³żČ„“ÖŃĪÖŠµÄSO42£”¢Ca2+”¢Mg2+µČŌÓÖŹ£¬¼ÓČėŅ©Ę·µÄĖ³ŠņĪŖ£ŗNa2CO3ČÜŅŗ”¢NaOHČÜŅŗ”¢BaCl2ČÜŅŗ”¢¹żĀĖŗó¼ÓŃĪĖį
B£®µŚ¢Ś²½µÄ¹Ų¼üŅŖµĶĪĀŠ”»šŗęøÉ
C£®ĀČ¼ī¹¤ŅµµÄŅõ¼«²śĪļŹĒCl2
D£®µŚ¢Ū²½µ½µŚ¢Ż²½µÄÄæµÄŹĒĪŖĮĖø»¼ÆäåŌŖĖŲ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģĪ÷²ŲČÕæ¦ŌņĒųµŚŅ»øß¼¶ÖŠŃ§øßČżÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĶʶĻĢā
·ÖA”¢B”¢C”¢D”¢EĪåÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£»AŌŖĖŲŹĒĖłÓŠŌ×ÓÖŠ°ė¾¶×īŠ”µÄŌ×Ó£»BŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļÓėĘäĒā»ÆĪļÉś³ÉŅ»ÖÖŃĪX£»DÓėAĶ¬Ö÷×壬ĒŅÓėEĶ¬ÖÜĘŚ£»EŌŖĖŲµÄ×īĶā²ćµē×ÓŹżŹĒĘä“ĪĶā²ćµē×ÓŹżµÄ3/4£¬A”¢B”¢D”¢EÕāĖÄÖÖŌŖĖŲÖŠ£¬ĆæŅ»ÖÖ¶¼ÓėCŌŖĖŲŠĪ³ÉŌ×ÓøöŹż±Č²»ĻąĶ¬µÄ»ÆŗĻĪļ”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)DĪ»ÓŚŌŖĖŲÖÜĘŚ±ķµŚ ÖÜĘŚ ×唣
(2)CŗĶEĮ½ŌŖĖŲĻą±Č½Ļ£¬·Ē½šŹōŠŌ½ĻĒæµÄŹĒ__________(ĢīŌŖĖŲĆū³Ę)£¬æÉŅŌŃéÖ¤øĆ½įĀŪµÄŹĒ_________________(ĢīŠ“±ąŗÅ)£»
A£®±Č½ĻÕāĮ½ÖÖŌŖĖŲµÄĘųĢ¬Ēā»ÆĪļµÄ·Šµć
B£®±Č½ĻÕāĮ½ÖÖŌŖĖŲµÄµ„ÖŹŌŚ³£ĪĀĻĀµÄדĢ¬
C£®±Č½ĻÕāĮ½ÖÖŌŖĖŲĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ
D£®±Č½ĻÕāĮ½ÖÖŌŖĖŲµ„ÖŹÓėĒāĘų»ÆŗĻµÄÄŃŅ×
(3)Š“³öC”¢DĮ½ŌŖĖŲŠĪ³ÉµÄŌ×ÓøöŹż±ČĪŖ1:1µÄ»ÆŗĻĪļÓėĖ®·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ ”£
(4)AÓėC¼äæÉŠĪ³ÉøŗŅ»¼ŪĖ«Ō×ÓŅõĄė×Ó£¬ÓŠ10øöµē×Ó£¬Š“³öøĆŅõĄė×ÓÓėŃĪĖį·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ £»
(5)A”¢C ”¢D”¢EĖÄÖÖŌŖĖŲæÉŠĪ³ÉĮ½ÖÖĖįŹ½ŃĪ£¬Į½ÖÖĖįŹ½ŃĪĻą»„·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ .
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģŗžÄĻŹ”øßČżÉĻѧʌ9ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
ÓĆĻĀĶ¼×°ÖĆæÉŅŌ½ųŠŠ²ā¶ØSO2×Ŗ»Æ³ÉSO3µÄ×Ŗ»ÆĀŹµÄŹµŃ飮ŅŃÖŖSO3µÄČŪµćŹĒ16£¬8”ę£¬·ŠµćŹĒ445.8”ę£®ŅŃÖŖ·¢Éś×°ÖĆÖŠĖłÉę¼°·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗNa2SO3£Øs£©+H2SO4£Ø98%£©ØTNa2SO4+H2O+SO2”ü
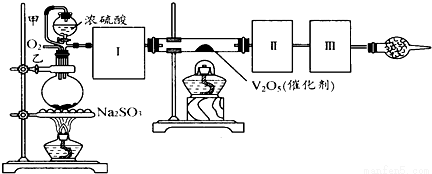
£Ø1£©øł¾ŻŹµŃéŠčŅŖ£¬Ó¦øĆŌŚ¢ń”¢¢ņ”¢¢ó“¦Į¬½ÓŗĻŹŹµÄ×°ÖĆ£®Ēė“ÓĻĀĶ¼A”«E×°ÖĆÖŠŃ”Ōń×īŹŹŗĻ×°ÖĆ²¢½«ĘäŠņŗÅĢīČėĻĀĆęµÄæÕøńÖŠ£®
¢ń”¢¢ņ”¢¢ó“¦Į¬½ÓµÄ×°ÖĆ·Ö±šŹĒ__________”¢__________”¢__________£®
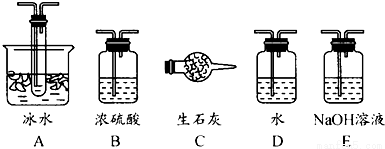
£Ø2£©“ÓŅŅ“¦¾łŌČĶØČėO2£¬ĪŖŹ¹SO2ÓŠ½ĻøßµÄ×Ŗ»ÆĀŹ£¬ŹµŃéÖŠŌŚ¼ÓČČ“ß»Æ¼ĮÓėµĪ¼ÓÅØĮņĖįµÄĖ³ŠņÖŠ£¬Ó¦²ÉČ”µÄ²Ł×÷ŹĒ__________________£®
£Ø3£©½«SO2ĶØČėŗ¬1.5molĀČĖįµÄČÜŅŗÖŠ£¬æÉÉś³ÉŅ»ÖÖĒæĖįŗĶŅ»ÖÖŃõ»ÆĪļ£¬ČōÓŠ1.5”Į6.02”Į1023øöµē×Ó×ŖŅĘŹ±£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½______________
£Ø4£©ÓĆamolNa2SO3·ŪÄ©Óė×ćĮæÅØĮņĖį½ųŠŠ“ĖŹµŃ飬µ±·“Ó¦½įŹųŹ±£¬¼ĢŠųĶØČėO2Ņ»¶ĪŹ±¼äŗ󣬲āµĆ×°ÖĆ¢óŌöÖŲĮĖbg£¬ŌņŹµŃéÖŠSO2µÄ×Ŗ»ÆĀŹĪŖ______%£ØÓĆŗ¬a”¢bµÄ“śŹżŹ½ĢīŠ“£©
£Ø5£©Ī²¶ĖĒņŠĪøÉŌļ¹ÜµÄ×÷ÓĆŹĒ__________________£®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com