
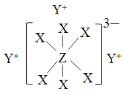
【题目】清代化学家徐寿创立了化学元素的中文名称和造字原则,推动了化学知识在中国的传播和应用。物质A由原子序数依次增大的短周期元素X、Y、Z组成,其中Z为金属元素,X、Y、Z简单离子的核外电子排布相同,物质A的结构式如图所示:
回答下列问题:
(1)Y、Z元素的名称为徐寿确定并使用至今,Y在周期表中的位置是__________。
(2)比较X、Y、Z简单离子的半径大小(用对应离子符号表示)__________。
(3)在YZO2与YX的混合液中,通入足量CO2是工业制取A的一种方法,写出该反应的化学方程式__________。
(4)与X同主族的元素溴和碘可以发生下列置换反应:Br2+2I-=2Br-+I2,I2+2BrO3-=2IO3-+Br2,这两个置换反应矛盾吗?简述理由__________。
【答案】第三周期第ⅠA族 F>Na+>Al3+ NaAlO2+6NaF+4CO2+2H2O=Na3AlF6+4NaHCO3 不矛盾。前者Br2是氧化剂,I2是氧化产物,氧化剂的氧化性大于氧化产物;后者I2是还原剂,Br2是还原产物,还原剂的还原性大于还原产物。(不矛盾;前者是“Br”得电子倾向强于“I”,后者是“I”失电子倾向强于“Br”)
【解析】
分析A的结构式,其中Y形成+1价的阳离子,X可形成一个共价键,Z成六个共价键,X、Y、Z为原子序数依次增大的短周期元素,其中Z为金属元素。由此可推断X形成-1价的阴离子,可推测X为F元素,根据X和Z形成显-3价的阴离子,可知Z应显+3价,且Z为金属元素,则Z为Al元素。由X、Y、Z简单离子的核外电子排布相同,可知Y为Na元素,据此进行分析。
(1)Na元素在元素周期表中位于第三周期第ⅠA族,答案为:第三周期第ⅠA族;
(2)根据核外电子排布相同时,核电荷数越大,离子半径越小,X、Y、Z简单离子的核外电子排布相同,则其离子半径大小关系为:F>Na+>Al3+;答案为:F>Na+>Al3+;
(3)根据题意及原子守恒,可知化学反应方程式为:NaAlO2+6NaF+4CO2+2H2O=Na3AlF6+4NaHCO3;答案为:NaAlO2+6NaF+4CO2+2H2O=Na3AlF6+4NaHCO3;
(4)不矛盾;分析两个反应,在前一个反应中,Br2作为氧化剂,将I-氧化为I2,I2为氧化产物,体现了氧化性:Br2>I2;在后一个反应中,BrO3-中Br的化合价降低,被还原为Br2,Br2为还原产物,I2作为还原剂,体现了还原性:I2>Br2。答案为:不矛盾;前者Br2是氧化剂,I2是氧化产物,氧化剂的氧化性大于氧化产物;后者I2是还原剂,Br2是还原产物,还原剂的还原性大于还原产物。(不矛盾;前者是“Br”得电子倾向强于“I”,后者是“I”失电子倾向强于“Br”)。


科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的容器中,对于反应 A(g)+2B(g)![]() 3C(g)(正反应为吸热反应),下列叙述为平衡状态标志的是
3C(g)(正反应为吸热反应),下列叙述为平衡状态标志的是
①体系的温度不再变化 ②外界条件不变时,A、B、C浓度保持不变 ③气体平均分子量不再变化 ④体系的压强不再变化 ⑤气体密度不再变化 ⑥3 v正(B)=2 v逆(C) ⑦单位时间内消耗1 mol A(g)的同时生成3 mol C(g)
A.①②⑥B.①②③⑤C.②③④⑤D.①②④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸发生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的说法中,正确的是( )
A. 苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B. 从苯的凯库勒式( )看,苯分子中含有碳碳双键,应属于烯烃
)看,苯分子中含有碳碳双键,应属于烯烃
C. 在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D. 苯分子为平面正六边形结构,6个碳原子之间的价键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)按官能团的不同,可以对有机物进行分类,请写出下列有机物的种类:
① CH3CH2CH2COOH ________; ② ![]() _________;
_________;
③ CH3CH2CHO _____________; ④ ![]() ________________。
________________。
(2)请用系统命名法命名下列有机物:
① CH3C(CH3)2CH2CH3 ________ ②![]() _________ ③
_________ ③  __________
__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由化合物A制备可降解环保塑料PHB和一种医药合成中间体J的合成路线如图:
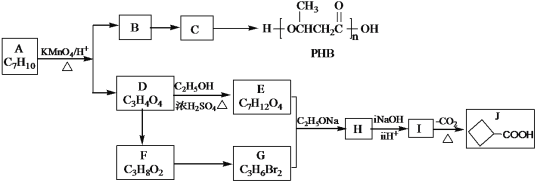
已知:
ⅰ.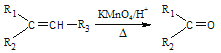 +R3—COOH(—R1、—R2、—R3均为烃基)
+R3—COOH(—R1、—R2、—R3均为烃基)
ⅱ.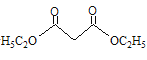 +2RBr
+2RBr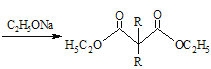 +2HBr
+2HBr
回答下列问题:
(1)C→PHB的反应类型是__________________。
(2)B中官能团的名称是__________________。
(3)A的结构简式是__________________。
(4)D→E的反应方程式是_____________________________。
(5)E+G→H的反应方程式是____________________________。
(6)X是J的同分异构体,满足下列条件的有_种(不考虑顺反异构)。
①链状结构;
②既能发生银镜反应,又能发生水解反应。
其中核磁共振氢谱有三组峰,且峰面积之比为6:1:1的结构简式是_________。
(7)已知:2CH3CHO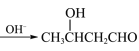 。
。
以乙烯为起始原料,选用必要的无机试剂合成C,写出合成路线__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二环[1,0,0]丁烷(![]() )是最简单的桥环化合物。下列关于该化合物的说法错误的是
)是最简单的桥环化合物。下列关于该化合物的说法错误的是
A. 该化合物的二溴代物有4种
B. 生成1molC4H10需要2molH2
C. 该化合物与1,3-丁二烯互为同分异构体
D. 该化合物中4个碳原子可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。回答下列问题:
(1)在周期表中,与Li的化学性质最相似的邻族元素是________,该元素基态原子核外M层电子的自旋状态_________(填“相同”或“相反”)。
(2)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为____,其中Fe的配位数为_____________。
(3) NH4H2PO4中P的_______杂化轨道与O的2p轨道形成 σ 键。
(4)NH4H2PO4和LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
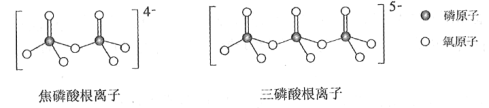
这类磷酸根离子的化学式可用通式表示为____________(用n代表P原子数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是
A. 从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构
B. 1 mol金刚石晶体中,平均含有2 mol C—C键
C. 水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键
D. 某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE
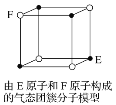
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com