
对复杂的有机物结构可用“键线式”表示。如苯丙烯酸1—丙烯酯: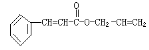 可简化为
可简化为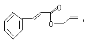 杀虫剂“阿乐丹”的结构表示为
杀虫剂“阿乐丹”的结构表示为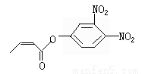 ,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
A.均能发生银镜反应 B.遇FeCl3溶液均显紫色
C.均能与NaHCO3溶液发生反应 D.均能与浓溴水发生反应
 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:选择题
16O和18O是氧元素的两种核素,用NA表示阿伏加德罗常数的数值,下列说法不正确的是( )A.在18g 16O2中含有NA个氧原子
B.16O与18O核外电子排布方式相同
C.在标准状况下,1.12L 16O2和1.12L 18O2均含有0.1NA个氧原子
D.18O 2和16O2化学性质几乎相同
2和16O2化学性质几乎相同
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一下期中化学试卷(解析版) 题型:选择题
能够说明氯的非金属性比硫强的事实有
①HCl酸性强于H2S的酸性
②将氯气通入H2S溶液中可置换出硫
③氯气与铁反应生成FeCl3,硫与铁反应生成FeS
④硫和氯变成简单阴离子时硫原子得到的电子更多
⑤氯气和氢气的混合气,经强光照射可剧烈反应,而硫与氢气反应需较高温度
A.②③⑤ B.①③⑤ C.①②③ D.①②③⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一下期中化学试卷(解析版) 题型:选择题
元素周期表是学习化学的重要工具,下图是元素周期表中的一格,以下对该图信息的解读中,不正确的是
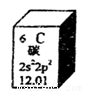
A.该元素的原子序数为6
B.该元素所有原子的质子数均为6
C.该元素的原子质量为12.01 g
D.该元素应有多种同位素,所有原子的中子数不都为6
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江双鸭山一中高二下期中化学试卷(解析版) 题型:实验题
某化学小组以苯甲酸为原料,制取苯甲酸甲酯.已知有关物质的沸点如下表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
沸点/℃ | 64.7 | 249 | 199.6 |
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入9.6ml(密度约为1.27g.ml-1)苯甲酸和20mL甲醇(密度约0.79g·mL﹣1),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1) 加入碎瓷片的作用是 ;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作时 (填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(2)浓硫酸的作用是 混合液体时最后加入浓硫酸的理由: 。
(3)甲、乙、丙三位同学分别设计了如图三套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点最好采用装置 (填“甲”或“乙”或“丙”)。
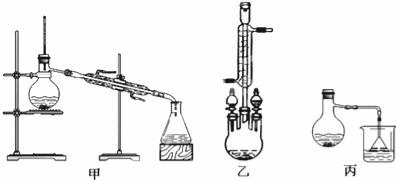
Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中含有少量甲醇、硫酸、苯甲酸和水,现拟用下列流程进行精制,请根据流程图写出操作方法的名称,操作Ⅱ 。
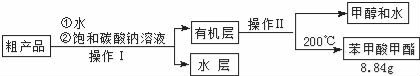
(5)不能用NaOH溶液代替饱和碳酸钠溶液的原因是 。
(6)列式计算,苯甲酸甲酯的产率是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江双鸭山一中高二下期中化学试卷(解析版) 题型:选择题
某有机物的结构简式为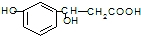 ,它可以发生反应的类型有( )
,它可以发生反应的类型有( )
①加成 ②消去 ③水解 ④酯化 ⑤氧化 ⑥加聚.
A.①②⑤⑥ B.③④⑤⑥ C.①②③④ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江双鸭山一中高二下期中化学试卷(解析版) 题型:选择题
由乙炔、苯和甲醛组成的混和物中,测得含碳元素的质量百分含量为72%,则混和物中氧元素的质量百分含量为( )
A 22% B 20.7% C 28% D 24.9%
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:选择题
下列说法错误的是
A.0.1 mol/L CH3COOH溶液中:c(CH3COO-)+c(CH3COOH)=0.1mol/L
B.将Al2(SO4)3溶液蒸干,灼烧得Al2O3
C.配制FeCl3溶液,应加少量盐酸
D.Na2S溶液中:c(OH-)=c(H+) + c(HS-) + 2c(H2S)
查看答案和解析>>
科目:高中化学 来源:2016届江西省、临川二中高三下联考理综化学试卷(解析版) 题型:实验题
钼酸钠晶体( Na2MoO4·2H2O)是一种无公害型冷却水系统的金属缓蚀剂。工业上利用钼精矿(主要成分是不溶于水的MoS2)制备钼酸钠的两种途径如图所示:

(1) NaClO的电子式是
(2)为了提高焙烧效率,除增大空气量外还可以采用的措施是
(3)途径I碱浸时发生反应的化学反应方程式为
(4)途径Ⅱ氧化时发生反应的离子方程式为
(5)分析纯的钼酸钠常用四钼酸铵[(NH4)2MoO4]和氢氧化钠反应来制取,若将该反应产生的气体与途径I所产生的尾气一起通入水中,得到正盐的化学式是
(6)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如下图:

①要使碳素钢的缓蚀效果最优,钼酸钠和月桂酰肌氨酸的浓度比应为____。
②当硫酸的浓度大于90%时,腐蚀速率几乎为零,原因是 。
③试分析随着盐酸和硫酸浓度的增大,碳素钢在两者中腐蚀速率产生明显差异的主要原因是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com