
| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2;△H(298K)=-242kJmol-1 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(l);△H(298K)=+484kJmol-1 | |
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g);△H(298K)=-242kJmol-1 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g);△H(298K)=-484kJ |
分析 2mol氢气燃烧生成水蒸气放出484kJ热量,则该反应的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol或H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ/mol,热化学方程式中必须标出各物质的状态,据此进行解答.
解答 解:A.水的分解为吸热反应,焓变值应该大于0,正确的热化学方程式为:H2O(g)═H2(g)+$\frac{1}{2}$O2;△H(298K)=+242kJmol-1,故A错误;
B.氢气的燃烧为放热反应,则焓变值小于0,正确的热化学方程式为:H2O(g)═H2(g)+$\frac{1}{2}$O2;△H(298K)=+242kJmol-1,故B错误;
C.2mol氢气燃烧生成水蒸气放出484kJ热量,则该反应的热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ/mol,故C正确;
D.该反应的焓变的数值、单位错误,正确的热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ/mol,故D错误;
故选C.
点评 本题考查了热化学方程式的书写方法,题目难度中等,明确热化学方程式的书写原则为解答关键,注意掌握化学反应与能力变化关系,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

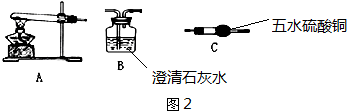

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2S是还原产物,反应中1 mol CuSO4失1 mol电子 | |
| B. | 5 mol FeS2发生反应,有10 mol电子转移 | |
| C. | 产物中的SO42-离子有一部分是氧化产物 | |
| D. | FeS2只作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有机物不能通过人工的方法合成 | |
| B. | 烃是指燃烧后只生成CO2和H2O的有机物 | |
| C. | 有机物只含有碳、氢两种元素 | |
| D. | 含碳元素的化合物不一定都属于有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
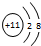 ,F中的化学键为离子键、共价键;
,F中的化学键为离子键、共价键;查看答案和解析>>
科目:高中化学 来源: 题型:推断题
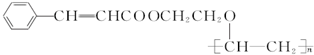 .按如图所示关系可以合成甲,其中试剂I可由乙醇与氧气在催化剂加热条件下反应得到.
.按如图所示关系可以合成甲,其中试剂I可由乙醇与氧气在催化剂加热条件下反应得到.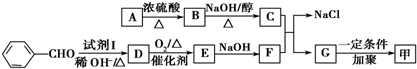
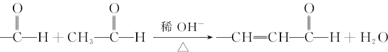
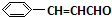 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2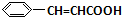 +H2O;
+H2O;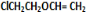 +
+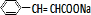 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$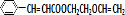 +NaCl.
+NaCl.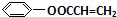 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3X2+Y2═2X3Y | B. | 2X2+Y2═2X2Y | C. | X2+2Y2═2XY2 | D. | X2+3Y2═2XY3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:| 乙醇 | 1,2-二溴乙烷 | 醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com