
| A. | 分离KNO3和氯化钠,常用结晶与重结晶 | |
| B. | 分离溴苯和水,常用蒸馏法 | |
| C. | 提纯含有碘的食盐,常用升华法 | |
| D. | 苯和酸性高锰酸钾溶液可用分液法 |
分析 A.KNO3和氯化钠的溶解度受温度影响不同;
B.溴苯和水不互溶,不互溶的液体采用分液方法分离;
C.碘易升华,食盐不能升华;
D.苯和酸性高锰酸钾溶液分层.
解答 解:A.KNO3和氯化钠的溶解度受温度影响不同,则利用结晶与重结晶分离,故A正确;
B.不互溶的液体采用分液方法分离,苯和溴苯不互溶,所以可以采用分液方法分离,故B错误;
C.碘易升华,食盐不能,则利用升华法提纯食盐,故C正确;
D.苯和酸性高锰酸钾溶液分层,利用分液法分离,故D正确;
故选B.
点评 本题考查物质分离和提纯,为高频考点,明确物质性质及分离方法关系是解本题关键,利用物质性质的差异性选取合适的方法分离,常见物质分离方法有:分液、蒸馏、过滤、渗析、盐析等,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 相同温度下,2 mol•L-1的醋酸溶液与1 mol•L-1的醋酸溶液中的c(H+)之比 | |
| B. | H2CO3水溶液中c(H+)与c(CO32-)之比 | |
| C. | Na2CO3溶液中c(Na+)与c(CO32-)之比 | |
| D. | 常温下,0.1 mol•L-1Na2CO3溶液与0.1 mol-1CH3COONa溶液中c(Na+)之比 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子是一种呈正四面体型的、含极性键的非极性分子 | |
| B. | 甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子 | |
| C. | 甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业 | |
| D. | “抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最外层电子数:C>D>A>B | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:Cn->D(n+1)->An+>B(n+1)+ | D. | 单质还原性:B>A>C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂和还原剂的物质的量之比为1:14 | |
| B. | 由该反应可知还原性:HCl>CrCl3 | |
| C. | 当转移0.2mol电子时,被氧化的还原剂的物质的量为0.2mol | |
| D. | Cl2是该反应的氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
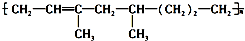 下列有关其叙述不正确的是( )
下列有关其叙述不正确的是( )| A. | 该高聚物是通过加聚反应生成的 | |
| B. | 合成该高聚物的单体有三种 | |
| C. | 1mol该物质能与1molH2加成,生成不含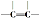 的物质 的物质 | |
| D. | 该高聚物能被酸性KMnO4溶液氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
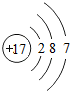 ;
; ,该化合物的水溶液在空气中久置后变质,生成一种单质和一种强碱,用化学方程式表示这一变化过程并用单线桥标记电子转移的方向和数目:
,该化合物的水溶液在空气中久置后变质,生成一种单质和一种强碱,用化学方程式表示这一变化过程并用单线桥标记电子转移的方向和数目: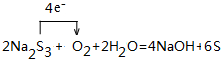
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com