
| A.自来水 | B.0.5mol·L-1盐酸 | C.0.5mol·L-1醋酸溶液 | D.0.5mol·L-1KCl溶液 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
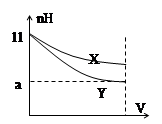
| A.X、Y两种碱的物质的量浓度一定相等 |
| B.稀释后,X溶液碱性比Y溶液碱性强 |
| C.若9<a<11,则X、Y都是弱碱 |
| D.完全中和X、Y两溶液时,消耗同浓度盐酸的体积V(X)>V(Y) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a的浓度必小于乙酸的浓度 | B.a的浓度必大于乙酸的浓度 |
| C.b的浓度必小于乙酸的浓度 | D.b的浓度必大于乙酸的浓度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| ① | HF | Ka=6.8×10-4 mol?L-1 |
| ② | CH3COOH | Ka=1.7×10-5 mol?L-1 |
| ③ | HCN | Ka=6.2×10-10 mol?L-1 |
| ④ | H2CO3 | Ka1=4.4×10-7mol?L-1 Ka2=4.7×10-11 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
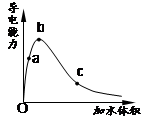
| A.a、b、c三点溶液的pH:a>b>c |
| B.若用湿润的pH试纸测试c处溶液的pH,比实际的pH偏小 |
| C.a、b、c三点溶液用1 mol/L的NaOH溶液中和,消耗NaOH溶液的体积a>b>c |
D.若在O点醋酸双聚成八元环。则其结构式为: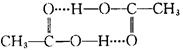 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.中和两者,需要pH相等的相同体积的NaOH溶液 |
| B.稀释两者相同倍数时,pH仍然相等 |
| C.加适量的醋酸钠晶体后,两溶液的pH均增大 |
| D.加足量的锌充分反应后,两溶液中产生的氢气一样多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电离程度相同 | B.pH值相同 |
| C.物质的量浓度相同 | D.c(OH-)相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com