
| V |
| Vm |
| 2.8L |
| 22.4L/mol |
| 1mol |
| 0.25mol |
| 1mol |
| 2 |
| 1mol |
| 3 |
| 1mol |
| 2 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
A、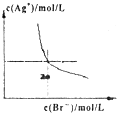 如图是某温度下将AgBr溶于水,c(Ag+)、c(Br-)的关系曲线,a点表示不饱和溶液 | B、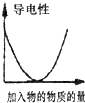 如图可能是在醋酸溶液中不断加入氨水,溶液的导电性情况 | C、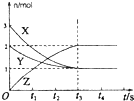 由图知,该反应的化学方程式为:3X+2Y=2Z | D、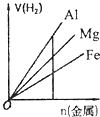 如图是可能镁、铝、铁与足量盐酸的反应,纵坐标表示的是生成氢气体积,横坐标表示的是三种金属的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源:2008-2009学年山东省临沂市费县高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目:高中化学 来源: 题型:
由镁、铝、铁三种金属单质中的两种组成的混合物共6g,与足量的稀盐酸反应,产生标准状况下的氢气2.8L,由此得出的结论中正确的是( )
A.混合物中一定含有铝 B.混合物中一定含有铁
C.该混合物一定是由铁和镁组成的 D.混合物中一定不含有铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com