

分析 根据题中各物质的转化关系可知,本实验是将溴苯先与镁反应生成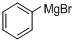 ,
, 与丁酮反应生成
与丁酮反应生成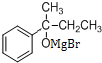 ,
, 再与酸反应生成
再与酸反应生成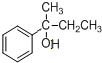 ,
,
(1)反应①是用溴苯与镁条反应,用碘作催化剂;
(2)装置Ⅰ中滴加液体用恒压漏斗,便于液体流下,反应②是放热反应,为防止反应过于剧烈,需将三颈烧瓶置于冰水中,且逐滴加入丁酮和乙醚;
(3)根据分液的基本步骤答题;
(4)减压蒸馏主要是防止温度过高物质发生分解,根据压蒸馏的操作要求答题.
解答 解:根据题中各物质的转化关系可知,本实验是将溴苯先与镁反应生成 ,
, 与丁酮反应生成
与丁酮反应生成 ,
, 再与酸反应生成
再与酸反应生成 ,
,
(1)反应①是用溴苯与镁条反应,用碘作催化剂,故答案为:作催化剂;
(2)装置Ⅰ中滴加液体用恒压漏斗,便于液体流下,反应②是放热反应,为防止反应过于剧烈,需将三颈烧瓶置于冰水中,且逐滴加入丁酮和乙醚,
故答案为:恒压漏斗;该反应放热,防止反应过于剧烈;
(3)步骤三中分离出油层,用分液操作即可,具体实验操作为:将混合液置于分液漏斗中,先放出下层液体于烧杯中,再将上层液体从上口倒入另一烧杯中,
故答案为:将混合液置于分液漏斗中,先放出下层液体于烧杯中,再将上层液体从上口倒入另一烧杯中;
(4)减压蒸馏时需将吸滤瓶与抽气泵相连,减压蒸馏主要是降低2-苯基-2-丁醇的沸点,防止温度过高发生分解,
故答案为:抽气泵;降低2-苯基-2-丁醇的沸点,防止温度过高发生分解.
点评 本题主要考查了有机物的制备实验方案设计,答题时注意根据实验原理进行分析,所以理解实验原理是解题的关键,题目难度中等,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.


科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z | W |
| T |
| A. | X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增 | |
| B. | Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | YX2晶体熔化、液态WX3气化均需克服分子间作用力 | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 生成物是乙醛 | B. | 乙醇发生了还原反应 | ||
| C. | 铜是此反应的催化剂 | D. | 反应中有红黑颜色交替变化的现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题


 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ +HCl(R、R1、R2均为烃基)
+HCl(R、R1、R2均为烃基)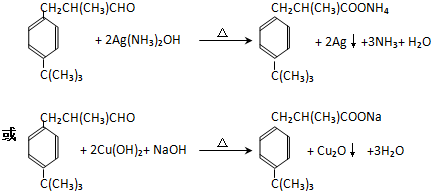 .
.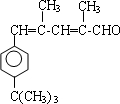 .
.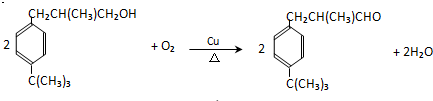 .
.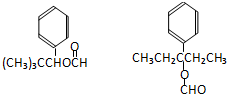 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 O3氧化海水中I-是大气中碘的主要来源.将O3通入稀硫酸酸化的NaI溶液中进行模拟研究,发生反应如下:
O3氧化海水中I-是大气中碘的主要来源.将O3通入稀硫酸酸化的NaI溶液中进行模拟研究,发生反应如下: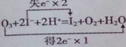 .
.| 实验编号 | 实验目的 | 反应物 | 温度 | 反应前溶液的pH |
| A | 对照组 | O3+NaI+H2SO4 | 25℃ | 5.2 |
| B | 研究FeCl2对I3-生成速率的影响 | O3+NaI+H2SO4+FeCl2 | 25℃ | 5.2 |
| C | 研究温度对I3-生成速率的影响 | O3+NaI+H2SO4 | 5℃ | 5.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
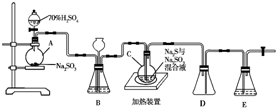 工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生产过程.烧瓶C中发生反应如下:
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生产过程.烧瓶C中发生反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
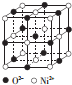 GTN{[Ni(CHZ)3](ClO4)2}是一种具有较强爆轰成长距离的初发药.
GTN{[Ni(CHZ)3](ClO4)2}是一种具有较强爆轰成长距离的初发药.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 淀粉和纤维素互为同分异构体 | |
| B. | 反应②:1 mol M可生成3 mol CH3CH2OH | |
| C. | 反应③:所需反应条件可为酸性重铬酸钾溶液 | |
| D. | 反应④:产物通入滴有酚酞的饱和碳酸钠溶液中振荡、静置后下层溶液颜色无变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)乙醇分子的结构式可表示如图1,在乙醇和钠反应时,③(填序号,下同)键断裂,在Cu催化和加热条件下与O2反应时,①②键断裂.
(1)乙醇分子的结构式可表示如图1,在乙醇和钠反应时,③(填序号,下同)键断裂,在Cu催化和加热条件下与O2反应时,①②键断裂.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com