
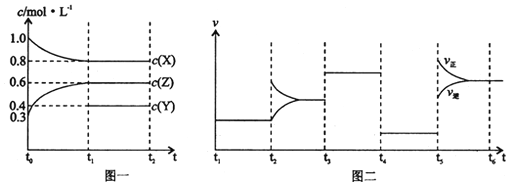
【题目】向1L的密闭容器中加入1molX、3molZ和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
A. Y的起始物质的量为0.5mol
B. 该反应的化学方程式为:2X(g)+Y(g)![]() 3Z(g)ΔH<0
3Z(g)ΔH<0
C. 若t0=0,t1=10s,则t0-t1阶段的平均反应速率为v(z)=0.03mol/(L﹒s)
D. 反应物X的转化率t6点比t3点高
【答案】B
【解析】A、t4-t5反应速率降低,但平衡不移动,说明t4时刻降低压强,即反应反应前后气体系数之和相等,x的浓度的变化(1-0.8)mol·L-1=0.2mol·L-1,Z的浓度的变化(0.6-0.3)mol·L-1=0.3mol·L-1,X和Z的系数之比为2:3,即Y的系数为1,Y的浓度变化为0.2/2mol·L-1=0.1mol·L-1,因此起始时Y的物质的量为(0.1+0.4)×1mol=0.5mol,故说法正确;B、根据选项A的分析,反应方程式2X(g)+Y(g) ![]() 3Z(g),根据图二,t5时刻应改变温度,正逆反应速率升高,因此t5是升高温度,反应向正反应方向进行,说明正反应是吸热反应,即△H>0,故说法错误;C、根据化学反应速率表达式,c(Z)=(0.6-0.3)/10mol/(L·s)=0.03 mol/(L·s),故说法正确;D、t5-t6时刻,平衡向正反应方向移动,X的转化率t6比t3高,故说法正确。
3Z(g),根据图二,t5时刻应改变温度,正逆反应速率升高,因此t5是升高温度,反应向正反应方向进行,说明正反应是吸热反应,即△H>0,故说法错误;C、根据化学反应速率表达式,c(Z)=(0.6-0.3)/10mol/(L·s)=0.03 mol/(L·s),故说法正确;D、t5-t6时刻,平衡向正反应方向移动,X的转化率t6比t3高,故说法正确。


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁均为中学化学常见的纯净物,它们之间有如图所示的反应关系。下列物质组不满足上述转化关系的是
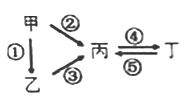
选项 | 甲 | 乙 | 丙 | 丁 |
A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
B | S | H2S | SO3 | H2SO4 |
C | N2 | NH3 | NO | NO2 |
D | Si | SiO2 | Na2SiO3 | Na2CO3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂方案错误的是( )
选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
A | C2H5OH | CH3COOH | 生石灰 | 蒸馏 |
B | Cl2 | HCl(g) | 饱和食盐水、浓H2SO4 | 洗气 |
C | NH4Cl溶液 | FeCl3 | NaOH溶液 | 过滤 |
D | 溴苯 | Br2 | NaOH溶液 | 振荡后分液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某白色粉未由两种物质组成,取少量样品加入足量水中,固体部分溶解,再向其中加入足量NaOH溶液,振荡,固体全部溶解;另取少量白色粉末加入足量硫酸,有气泡产生且有淡黄色不溶物生成。则该白色粉末可能为
A. N a2CO3、CaO B. Na2S2O3、Al2O3 C. Na2O2、Al(OH)3 D. NaI、AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)浓硫酸与木炭在加热条件下反应的化学方程式是___________________
(2)试用下图所列各种装置设计一个实验来验证上述反应所产生的各种产物。

这些装置的连接顺序,按产物气流从左到右的方向是(填装置的编号):
_________→________→________→__________。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。
A瓶溶液的作用是________________________________________,
C瓶溶液的作用是_________________________________________。
(4)装置②中所装的固体药品是_____________,可以验证的产物是_______
(5)装置③中所盛溶液是_______________,可以验证的产物是_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:氢氧化镁能溶于浓度均为3mol/L的①盐酸②NH4Cl溶液③醋酸铵溶液(中性),下列说法正确的是( )
A. c(NH4+):③>②
B. pH:①>②>③
C. Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s)![]() Mg2+(aq)+2OH-(aq)向溶解方向移动
Mg2+(aq)+2OH-(aq)向溶解方向移动
D. 等体积①和③混合溶液中c(Cl-)>c(NH4+)>c(H+)>c(CH3COO-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,我国储氢碳管研究获得重大进展,电弧法合成碳纳米管,常伴有大量物质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
3C + 2K2Cr2O7 + 8H2SO4(稀)= 3CO2↑ + 2K2SO4 + 2Cr2(SO4)3 + 8 H2O
请回答下列问题。
(1)H2O的摩尔质量为___________,0.18g H2O的物质的量为_______________mol
(2)配制0.1mol/L H2SO4溶液500mL,则需要H2SO4的质量为_____________g
(3)在上述的反应中,若生成22g CO2
ⅰ.标准状况下,CO2的体积为_________L
ⅱ.转移电子的数目为________________
(4)标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,则该混合气体的平均相对分子质量是_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或很少污染,且有些可以再生。下列属于新能源的是:①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥地热能 ⑦风能 ⑧氢能( )
A.①②③④ B.⑤⑥⑦⑧ C.③④⑤⑥ D.除①②外
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com