
【题目】将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g) === xC(g)+2D(g);5 min后测得c(D)=0.5 mol·L-1,c(A)∶c(B)=3∶5,C的反应速率是0.1 mol·L-1·min-1。
(1)A在5 min末的浓度是____________;
(2)v(B)=____________;
(3)x=____________。
【答案】0.75 mol·L-10.05 mol·L-1·min-12
【解析】
D的浓度为0.5mol/L,所以D的物质的量为1mol。
设A、B的物质的量为nmol,
3A(g)+B(g)![]() xC(g)+2D(g),
xC(g)+2D(g),
开始 n mol n mol 0 0
反应 1.5mol 0.5mol 1mol
5min (n-1.5)mol ( n-0.5)mol 1mol
c(A):c(B)=![]() :
:![]() =3:5,所以n=3;
=3:5,所以n=3;
(1)A在5min末的物质的量为:(n-1.5)mol=1.5mol,其物质的量浓度为![]() =0.75mol/L;
=0.75mol/L;
(2)C的反应速率是0.1molL-1min-1,根据同一反应中,各物质的反应速率之比等于计量数之比,所以B的反应速率是0.05molL-1min-1;
(3)D的浓度为0.5mol/L,反应时间为5min,D的反应速率为0.1molL-1min-1,C的反应速率是0.1molL-1min-1,根据同一反应中,各物质的反应速率之比等于计量数之比,所以x=2。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】利用下列实验装置进行相应的实验(部分夹持装置略去),不能达到实验目的的是
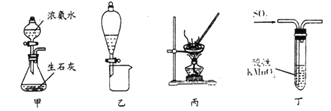
A. 利用图甲装置可快速制取少量氨气
B. 利用图乙装置分离水和溴的苯溶液
C. 利用图丙装置蒸发KCl溶液得晶体
D. 图丁装置中溶液颜色变浅,说明SO2具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴的化合物在磁性材料生产、电池制造、催化剂制备等方面应用十分广泛。
(1)二价钴离子的核外电子排布式为______。基态Co原子核外3d能级上有______个未成对电子。Co与Ca属同周期,且核外最外层电子构型相同,但金属钴熔沸点都比钙高,原因是______。
(2)0.1mol[Co(NO2)6]3-中所含的σ键数目是______,K3[Co(NO2)6]中K、N、O三种元素的第一电离能由大到小的顺序是______。
(3)化合物四氨基钴酞菁分子的结构式如图。四氨基钴酞菁中N原子的杂化轨道类型为______。
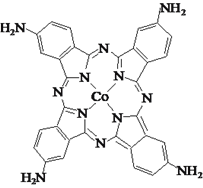
(4)[Co(NH3)6]Cl3晶体可由CoCl2溶于氨水并通入空气制得,该配合物中配体分子的立体构型是______。
(5)一种钴的化合物可用作石油脱硫的催化剂,其晶胞结构如图所示,则晶体中与每个O2-紧邻的O2-有______个,该钴的化合物的化学式是______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制备金属钛。下列说法正确的是

A. 电解过程中,Ca2+向阳极移动
B. 阳极的电极反应式为: C+2O2--4e-=CO2↑
C. 在制备金属钛前后,整套装置中CaO的总量减少
D. 若用铅蓄电池作该装置的供电电源,“+”接线柱连接的是Pb电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或事实与预期实验目的或所得结论对应正确的是
选项 | 实验操作或事实 | 实验目的或结论 |
A | 淡黄色试液 | 说明原溶液中一定含有Fe3+ |
B | 向AgNO3溶液中滴加过量氨水,溶液澄清 | Ag+与NH3H2O能大量共存 |
C | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变蓝 | NH4HCO3显碱性 |
D | H3PO3+2NaOH(足量)=Na2HPO3+2H2O | H3PO3属于二元酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图进行反应.下列说法中不正确的是

A. A、B、C中三种元素的任意两种元素形成的化合物所属物质类别可能是氧化物
B. A、B、C中三种元素形成的化合物所属物质类别一定不是碱
C. 如果E溶液是一种强酸,则E溶液为盐酸
D. A、B、C中有一种金属且为A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图海水综合利用的工业流程图,判断下列说法正确的是

已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
A. 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
B. 在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2
C. 在过程④、⑥反应中每氧化0.2molBr-需消耗2.24LCl2
D. 过程①的提纯是物理过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于ⅦA族元素的说法中,不符合递变规律的是( )
A.F2、Cl2、Br2、I2的氧化性逐渐减弱
B.F-、Cl-、Br-、I-的还原性逐渐增强
C.HF、HCl、HBr、HI的稳定性逐渐减弱
D.HF、HCl、HBr、HI水溶液的酸性逐渐减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com