
【题目】某实验小组探究SO2与AgNO3溶液的反应,实验记录如下:
序号 | Ⅰ | Ⅱ | Ⅲ |
实验 步骤 |
|
|
|
实验现象 | 得到无色溶液a和白色沉淀b | 产生无色气体,遇空气变为红棕色 | 产生白色沉淀 |
下列说法正确的是
A.透过测Ⅰ中无色溶液a的pH可以判断SO2是否被氧化
B.实验Ⅱ说明白色沉淀b具有还原性
C.实验Ⅲ说明溶液a中一定有![]() 生成
生成
D.实验Ⅰ、Ⅱ、Ⅲ说明SO2与AgNO3溶液反应既有Ag2SO4生成,又有Ag2SO3生成
【答案】B
【解析】
A.实验Ⅰ中,将SO2通入AgNO3溶液(pH=5)中得到无色溶液a,该溶液中可能含有亚硫酸,亚硫酸为中强酸,所以测定无色溶液a的pH无法判断二氧化硫是否被氧化,故A错误;
B.实验Ⅱ中,取白色沉淀B,加入3mol/LHNO3,产生的无色气体遇空气变成红棕色,说明硝酸被还原为NO,证明该沉淀B中含有还原性的物质存在,故B正确;
C.实验Ⅲ中,检验硫酸根离子应先加入盐酸酸化,目的是排除Ag+等,以免干扰硫酸根的检验,直接向溶液a中加入BaCl2,产生的沉淀可能为氯化银,不一定是硫酸根离子,故C错误;
D.由于实验Ⅰ、Ⅱ、Ⅲ不能证明产物中含有硫酸根,因此不能确定产物中含有Ag2SO4生成,故D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】下列实验方案设计中,无法达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 除去NaCl固体中少量的KNO3杂质 | 将固定溶于水配成溶液,蒸发结晶并趁热过滤 |
B | 检验乙酸乙酯中是否含有乙酸 | 加入含有酚酞的NaOH溶液并振荡,观察下层溶液颜色变化 |
C | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中滴入BaCl2溶液,观察溶液的变化 |
D | 比较Fe3+和I2的氧化性强弱 | 向含有淀粉的KI溶液中滴入FeCl3溶液,观察溶液颜色变化 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池是最常见的二次电池。由于铅蓄电池的性能优良、价格低廉、安全可靠,可多次充放电,所以在生产生活中使用广泛,汽车等机动车辆多数都使用这种蓄电池。
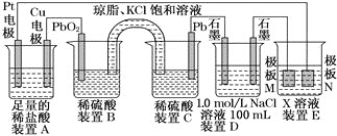
(1)装置B中PbO2上发生的电极反应方程式为______________。
(2)装置A中总反应的离子方程式为____________。
(3)盐桥中的______(填离子符号)向装置C中溶液方向移动。
(4)若装置E中的目的是精炼铜,则X为________,极板M的材料为________(填“粗铜”或“精铜”)。M电极质量改变6.4g时,N极质量变化_________6.4g,(填“大于”、 “小于”、“等于”或“无法确定”),装置D中产生的气体体积为_______L(标准状况下),溶液的pH______(填“增大”或“减小”,忽略溶液体积变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Fe3O4/Pd为催化材料,利用电化学原理实现H2消除酸性废水中的![]() ,其反应过程如图所示[已知Fe3O4中Fe元素化合价为+2、+3价,分别表示为Fe(Ⅱ)、Fe(Ⅲ)]。下列说法错误的是
,其反应过程如图所示[已知Fe3O4中Fe元素化合价为+2、+3价,分别表示为Fe(Ⅱ)、Fe(Ⅲ)]。下列说法错误的是
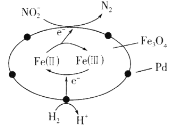
A.处理![]() 的电极反应为2NO2-+8H++6e-=N2↑+4H2O
的电极反应为2NO2-+8H++6e-=N2↑+4H2O
B.Fe(Ⅱ)与Fe(Ⅲ)的相互转化起到了传递电子的作用
C.用该法处理后,水体的pH降低
D.消耗标准状况下6.72LH2,理论上可处理含NO2-4.6mg·L-1的废水2m3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)命名下列有机物:
CH3CHOHCH3____________
HOCH2CH2CHO____________
 _________________
_________________
(2)燃烧某有机物A 1.50 g,生成1.12 L(标准状况)CO2和0.05 mol H2O,该有机物的蒸气对空气的相对密度是1.04,则该有机物的分子式为_____。
(3)已知端炔烃在催化剂存在下可发生偶联反应:![]() +H2, 称为Glaser反应,回答下列问题:
+H2, 称为Glaser反应,回答下列问题:
已知: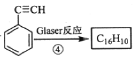 ,该转化关系的产物E(C16H10)的结构简式是_______,用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气____mol。
,该转化关系的产物E(C16H10)的结构简式是_______,用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气____mol。
(4)已知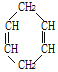 可简写为
可简写为 ,现有某化合物W的分子结构可表示为
,现有某化合物W的分子结构可表示为![]()
![]() 的一氯代物有______种
的一氯代物有______种![]()
![]() 下列有关W的说法不正确的是______
下列有关W的说法不正确的是______![]() 填编号
填编号![]() ;
;
a.能发生还原反应
b.能发生氧化反应
c.等质量的W与苯分别完全燃烧所消耗的氧气量,前者大
d.与苯互为同分异构体
![]() 写出W的芳香族同分异构体
写出W的芳香族同分异构体![]() 能发生聚合反应
能发生聚合反应![]() 的结构简式_________;该聚合反应的化学方程式为_________;
的结构简式_________;该聚合反应的化学方程式为_________;
![]() 属于______
属于______![]() 填编号
填编号![]() 。
。
![]() 芳香烃
芳香烃![]() 环烃
环烃![]() 不饱和烃
不饱和烃![]() 炔烃
炔烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子,Y原子是最轻的原子,人们曾预言它可能是所有元素之母。
(1)X基态原子的电子排布式为___。
(2)C、H、O、N四种原子的电负性由大到小的顺序为___。
(3)Y负离子基态电子排布式为___。
(4)下列变化:H-(g)=H(g)+e-吸收的能量为73kJ/mol,H(g)=H+(g)+e-吸收的能量为1311kJ/mol,则氢负离子的第一电离能为__。
(5)水溶液中有H3O+、H5O![]() 、H9O
、H9O![]() 等微粒的形式。H3O+中,中心原子的杂化类型是__,请画出H5O
等微粒的形式。H3O+中,中心原子的杂化类型是__,请画出H5O![]() 的结构式:__。
的结构式:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)制取铜的操作流程如下:

已知:Cu2O+2H+===Cu+Cu2++H2O
(1)实验操作Ⅰ的名称为_________;在空气中灼烧固体混合物D时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有________(填仪器名称)。
(2)滤液A中铁元素的存在形式为________(填离子符号),生成该离子的离子方程式为__________,检验滤液A中存在该离子的试剂为_____________(填试剂名称)。
(3)金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为___________
(4)常温下,等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH=________。
(5)利用电解法进行粗铜精炼时,下列叙述正确的是__________(填代号)。
a 电能全部转化为化学能
b 粗铜接电源正极,发生氧化反应
c 精铜作阴极,电解后电解液中Cu2+浓度减小
d 粗铜精炼时通过的电量与阴极析出铜的量无确定关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一氧化碳-空气燃料电池的工作原理示意图,a、b均为惰性电极。下列叙述中,正确的是( )
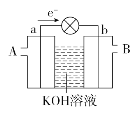
A. a电极发生还原反应,b电极发生氧化反应
B. a电极的电极反应式为CO+4OH-+2e-===CO32-+2H2O
C. A处通入的是空气,B处通入的是CO
D. 用该电池作电源精炼铜,若阴极质量增加6.4 g,至少消耗标准状况下的CO 2.24 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2 L的恒容密闭容器中发生反应![]() 。反应过程中的部分数据如下表所示:
。反应过程中的部分数据如下表所示:
n/mol t/min |
|
|
|
0 | 2.0 | 2.4 | 0 |
5 | 0.9 | ||
10 | 1.6 | ||
15 | 1.6 |
下列说法正确的是( )
A.0~5 min用A表示的平均反应速率为![]()
B.该反应在10 min后才达到平衡
C.平衡状态时,![]()
D.物质B的平衡转化率为20%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com