
分析 (1)化合物中正负化合价的代数和为0;氧化铁与盐酸反应生成氯化铁,氯化铁与NaOH反应生成红褐色沉淀Fe(OH)3,铁离子在热水中水解生成Fe(OH)3胶体,丁达尔现象为胶体特有的性质;
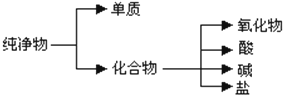
(2)由图可知,存在包含关系,为树状分类法;A中二氧化硅为酸性氧化物,B中氢氧化铝为两性氢氧化物,分别与其它两种不同类;CO32-+2H+═CO2↑+H2O表示可溶性碳酸盐与强酸反应生成可溶性盐、水、二氧化碳的反应,以此来解答.
解答 解:(1)合物中正负化合价的代数和为0,则Na2FeO4中Fe元素的化合价为0-(-2)×4-(+1)×2=+6;Fe2O3中Fe元素的化合价为+3,FeO中Fe元素的化合价为+2;取少量某油漆的原料Fe2O3(红棕色粉末)并加入适量浓盐酸,反应后得到棕黄色的溶液,取少量棕黄色溶液置于试管中,滴入NaOH溶液,可观察到有沉淀生成,生成沉淀的离子方程式为Fe3++3OH-═Fe(OH)3↓.另在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入2mL 上述棕黄色溶液,继续加热至液体呈红褐色,停止加热,证明所得分散系类型的实验方法的名称是丁达尔效应,
故答案为:+6;+3;+2;Fe3++3OH-═Fe(OH)3↓;红褐;丁达尔效应;
(2)由图可知,存在包含关系,为树状分类法,则选B;A中二氧化硅为酸性氧化物,其它两种为碱性氧化物,而B中氢氧化铝为两性氢氧化物,其它两种为碱;CO32-+2H+═CO2↑+H2O表示可溶性碳酸盐与强酸反应生成可溶性盐、水、二氧化碳的反应,如Na2CO3+2HCl═2NaCl+H2O+CO2↑,
故答案为:B;SiO2;Al(OH)3;Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评 本题考查物质的分类及胶体制备、元素化合价计算等,综合性较强,注重基础知识的考查,把握相关概念、分类方法为解答的关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
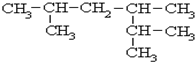
 ;
;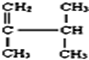 系统名称为2,3-二甲基-1-丁烯;
系统名称为2,3-二甲基-1-丁烯;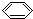 -C≡C-CH=CH-CH3,共面的碳原子最多有12个,共线的碳原子最多有6个.
-C≡C-CH=CH-CH3,共面的碳原子最多有12个,共线的碳原子最多有6个.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na放入水中,产生气体:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 在澄清的石灰水中通入过量SO2:SO2+OH-═HSO3- | |
| C. | Al片与少量NaOH溶液反应,产生气体:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | 次氯酸钙溶液中通入少量SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒 | |
| B. | 反应①中,NaCl是氧化产物 | |
| C. | 反应①为氧化还原反应,反应②为复分解反应 | |
| D. | 若有2mol FeCl3发生反应,转移电子的物质的量为6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
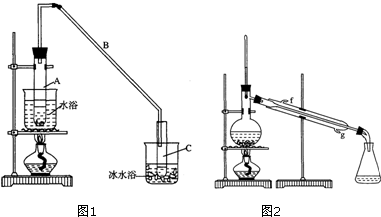
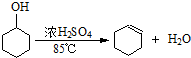
| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
 、SO2、CO2及水蒸气,混合气体通过试剂的顺序是④⑤①⑤②③(或④⑤①⑤③②) (填序号)
、SO2、CO2及水蒸气,混合气体通过试剂的顺序是④⑤①⑤②③(或④⑤①⑤③②) (填序号)查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下11.2L的水中含有0.5个NA水分子 | |
| B. | 0.1mol•L-1 NaCl溶液中Na+的数目为0.1NA | |
| C. | 1mol H2和O2的混合气体中含NA个分子 | |
| D. | 在常温常压下,18克水含有的原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 凡含有食品添加剂的食物对人体健康均有害,不可食用 | |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 | |
| D. | 酸钡难溶于水和酸,可做X光透视肠胃的药剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com