
| 0.01mol/L×2-0.01mol/L |
| 2 |
| 1×10-14 |
| 0.005 |


科目:高中化学 来源: 题型:
| A、中子数相同 |
| B、分子数不同 |
| C、质子数相同 |
| D、气体质量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③⑥ | B、③⑥ |
| C、①②④ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
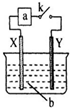
| A、当a为电流表,b为浓硝酸时:Y为负极 |
| B、当a为电流表,b为稀硫酸时:X电极反应为:Fe-2e-=Fe2+ |
| C、当a为直流电源,b为CuSO4溶液时:X、Y两电极附近的 SO42-浓度相等 |
| D、当a为直流电源,b为NaOH溶液,X极附近产生白色沉淀时:电子从X极流出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com