
����˵������ȷ����
A�������ԭˮ����ȵ��ˮ��������ܻ�����������
B��������ˮ(��NH4+��NH3)���û�ѧ��������绯ѧ����������
C��ij�ֹ�ѧ��⼼�����м��ߵ������ȣ��ɼ�����ϸ��(V=10��12L)�ڵ�����Ŀ����ӣ��ݴ˿�����ü�⼼���ܲ�����ϸ����Ũ��ԼΪ10��12��10��11mol ·L��1��Ŀ�����
D�������������Ӽ״��û��ȼ�ϵ���ֵ����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����±�����봼��˵������ȷ���ǣ� ��
A��±�����봼������ȥ��Ӧ��������ͬ
B�� 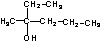 �ȿ��Է�����ȥ��Ӧ���ֿ��Ա�������������
�ȿ��Է�����ȥ��Ӧ���ֿ��Ա�������������
C����ͬ��±����ͨ����ȥ��Ӧ���ܻ�������ͬ��ϩ��
D��C2H5Br���Է�����ȥ��Ӧ����ô(CH3)3CBrҲ���Է�����ȥ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£�������Һ������Ũ�ȴ�С��ϵ��ȷ����
A��Na2S��Һ��c(Na+)>c(HS-)>c(OH-)>c(H2S)
B��Na2C2O4��Һ�У�c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)
C��Na2CO3��Һ��c(Na+)+c(H+)=2c(CO32-)+c(OH-)
D��CH3COONa��CaCl2�����Һ��c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������Ҫ������Դ��������Ϊ�������õĹؼ��������ǵ�ǰ��ע���ȵ�֮һ��
�������������Դ����ȼ�ղ���Ϊ ��
��NaBH4��һ����Ҫ�Ĵ������壬����ˮ��Ӧ����NaBO3���ҷ�Ӧǰ��B�Ļ��ϼ۲��䣬�÷�Ӧ�Ļ�ѧ����ʽΪ����Ӧ����1molNaBH4ʱת�Ƶĵ�����ĿΪ��
�Ǵ���ɽ����л�������û�����ͱ�֮��Ŀ��淴Ӧ��ʵ������ͼ��⡣

 (g)
(g)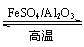


 (g)��3H2(g)
(g)��3H2(g)
��ij�¶��£�����������м��뻷���飬����ʼŨ��Ϊamol��L��1��ƽ��ʱ����Ũ��Ϊbmol��L��1���÷�Ӧ��ƽ�ⳣ��K��
��һ�������£���11ͼ��ʾװ�ÿ�ʵ���л���ĵ绯ѧ���⣨���������л����


�ٵ����е���ת�Ʒ���Ϊ ������A��D��ʾ��
������Ŀ�����ĵ缫��ӦʽΪ ��
�۸ô���װ�õĵ���Ч�ʦǣ� �����ǣ�����Ŀ��������ĵĵ�����/ת�Ƶĵ���������100%������������С�����1λ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ͼ��ʾװ�ý�������ʵ�飬�ܵó���Ӧʵ����۵���
| �� | �� | �� | ���� |
| |
| A | ϡ���� | Na2S | AgNO3�� AgCl����Һ | Ksp(AgCl)>Ksp(Ag2S) | |
| B | Ũ���� | ���� | ��ˮ | Ũ���������ˮ�ԡ������� | |
| C | ϡ���� | Na2SO3 | Ba(NO3)2 ��Һ | SO2������Ա��ξ������� ��ɫ���� | |
| D | Ũ���� | Na2CO3 | Na2SiO3��Һ | ���ԣ�����>̼��>���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������ˮ�����г�����ɱ��������HClO��ɱ��������ClO��ǿ��25��ʱ����-��ˮ��ϵ�д�������ƽ���ϵ��
Cl2(g)  Cl2(aq) K1=10��1.2
Cl2(aq) K1=10��1.2
Cl2(aq)+ H2O  HClO + H+ +Cl�� K2=10��3.4
HClO + H+ +Cl�� K2=10��3.4
HClO  H+ + ClO�� Ka=?
H+ + ClO�� Ka=?
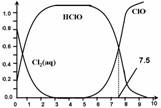 ����Cl2(aq)��HClO��ClO���ֱ�����������ռ����(��)��pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�����ȷ����
����Cl2(aq)��HClO��ClO���ֱ�����������ռ����(��)��pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�����ȷ����
A��Cl2(g)+ H2O  2H+ + ClO�� + Cl�� K=10��10.9
2H+ + ClO�� + Cl�� K=10��10.9
B�����ȴ���ˮ��ϵ�У�c(HClO) + c(ClO��) =c(H+)��c(OH��)
C�����ȴ�������ˮʱ��pH=7.5ʱɱ��Ч����pH=6.5ʱ��
D���ȴ�������ˮʱ�����ļ���ɱ��Ч�����ڶ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ж�����˵���Ƿ���ȷ��������ȷ��˵�����ɡ�
��Ԫ������Ȼ���еĴ�����ʽ��ԭ�ӡ����ӻ�����
���ڻ�ѧ�仯�У����ӿ����ٷ֣����Ӻ�ԭ�Ӳ������ٷ�
��ͬһ��Ԫ�ؿ����ж��ֲ�ͬԭ�ӣ�ͬһ��ԭ��Ҳ�����γɲ�ͬ������
��ԭ�����ԭ���γɵ��������ԭ�������������
����ͬһ��Ԫ����ɵ�����һ����ͬһ������
�����ʵĻ�ѧ����һ�����ɷ��ӱ��ֵ�
�����������������͵���������ͬ������һ����ͬһ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
500 mL 2 mol��L��1 FeCl3��Һ��500 mL 2 mol��L��1������Һ�ֱ�����ˮ�У������Ƴɷ�ɢϵ�ס��ң����ⶨ����ɢϵ�з�ɢ�ʵ�����ֱ����С��1��100 nm֮�䣬�ҷ�ɢϵ�з�ɢ�ʵ�����ֱ����С��10��9��10��7 m֮�䡣���й��ڼס��ҷ�ɢϵ���жϺ�������
(����)
A���ڰ�������һ�������ġ�ǿ�⡱����ס��ң����ּ��ж����ЧӦ����û�ж����ЧӦ
B����ס����зֱ�μӹ���������������Һ�������ǡ��Ⱦ۳������ܽ⡱
C����ס����зֱ�μӹ���������ᣬ��������ֱ������ɫ��Һ����ɫ��Һ
D�����ɡ�����FeCl3��Һ���� ����Һ��õ���Ӧ�Ĺ�����
����Һ��õ���Ӧ�Ĺ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ���� (����)
A��MnO2��Ũ���ᷴӦ��Cl2��MnO2��4HCl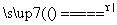 Mn2����2Cl����Cl2����2H2O
Mn2����2Cl����Cl2����2H2O
B����������ˮ����Al(OH)3���壺Al3����3H2O===Al(OH)3����3H��
C��Na2O2����ˮ����O2��Na2O2��H2O===2Na����2OH����O2��
D��Ca(HCO3)2��Һ������NaOH��Һ��Ӧ��HCO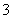 ��Ca2����OH��===CaCO3����H2O
��Ca2����OH��===CaCO3����H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com