
【题目】改变0.1 mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示[已知![]() ]。下列叙述不正确的是( )
]。下列叙述不正确的是( )

A.NaHA溶液中,HA-的水解能力小于HA-的电离能力
B.lg[K2(H2A)]=-4.2
C.将等物质的量的NaHA和Na2A混合物溶于水,所得的溶液中α(HA-)=α(A2-)
D.0.1 mol·L1 NaHA溶液中:c(Na+)+c(A2)+c(H2A)+c(HA)=0.2 mol·L1
【答案】C
【解析】
A.pH=4.2时,c(H+)=10-4.2mol·L-1,c(HA-)=c(A2-),K2(H2A)=c(A2-)·c(H+)/c(HA-)=10-4.2;pH=1.2时c(H2A)=c(HA-),则Kh(HA-)=c(OH-)·c(H2A)/c(HA-)=c(OH-)=10-12.8<10-4.2,说明HA-的水解能力小于HA-的电离能力,故A正确;
B.pH=4.2时,c(H+)=10-4.2mol·L-1,c(HA-)=c(A2-),K2(H2A)=c(A2-)·c(H+)/c(HA-)=10-4.2,则lg[K2(H2A)]=-4.2,故B正确;
C.将等物质的量的NaHA和Na2A混合物溶于水,由于NaHA的电离程度和Na2A的水解程度不同,所得的溶液中α(HA-)与α(A2-)不相等,故C错误;
D.根据0.1 mol·L-1 NaHA溶液中的物料守恒可知:c(Na+)+c(A2-)+c(H2A)+c(HA-)=0.2 mol·L-1,故D正确;
故选C。


科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素A、B、C、D、E,原子序数依次增大,A和B是组成物质种类最多的元素,C是地壳中含量最多的元素,D与B同族,E的3d轨道中有9个电子。
(1)C、D两种元素形成的化合物统称硅石,可通过__方法区分其结晶形和无定形的两种存在形态,C的电子排布图为___。
(2)M和N是生活中两种常见的有机物,M能与CaCO3反应,可用于厨房除水垢;N分子中的碳原子数目与M中相同,二者互为同分异构体,可发生银镜反应。M中存在化学键的类型是__;
A.离子键 B.极性键 C.非极性键 D.σ键 E.π键
N分子官能团中碳原子的轨道杂化类型是__。
(3)第一电离能:B___D(用“>”或“<”表示,下同);熔点:DC2晶体___D晶体。
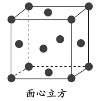
(4)E单质为面心立方晶体,其原子半径为Rcm,其晶胞棱长为anm,则E单质的密度为___g·cm-3(用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列有机物的系统命名或结构简式。
(1)![]() ___;
___;
(2)![]() ___;
___;
(3)CH3CH(CH3)C(CH3)2(CH2)2CH3___;
(4)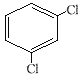 ___;
___;
(5)2,5-二甲基-4-乙基庚烷__;
(6)2-甲基-2-戊烯____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.CH3COOCH2CH3 与CH3CH2COOCH3 中均含有甲基、乙基和酯基,为同一种物质
B.![]() 和
和 ![]() 为同一物质
为同一物质
C.CH3CH2CH2CH2CH3 和CH3CH2CH(CH3)2 互为同素异形体
D.CH3CH2OH 和 CH2OHCHOHCH2OH 具有相同的官能团,互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用“银-Ferrozine”法检测室内甲醛含量的原理如下:

下列说法错误的是
A.标准状况下,11.2 L CO2中含C=O键的数目为6.02×1023
B.反应①的化学方程式为2Ag2O+HCHO=4Ag+CO2↑+H2O
C.理论上吸收HCHO与消耗Fe3+的物质的量之比为4:1
D.30 g HCHO被氧化时转移电子数目为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Fe、FeO和Fe2O3的混合物中加入60mL 4 mol·L-1的稀硝酸,恰好使混合物完全溶解,放出1.344 L NO(标准状况),往所得溶液中加入KSCN溶液,无红色出现.若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为
A.0.09 molB.0.12 molC.0.16 molD.0.21 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蒽(![]() )与苯炔(
)与苯炔(![]() )反应生成化合物X(立体对称图形),如图所示:
)反应生成化合物X(立体对称图形),如图所示:
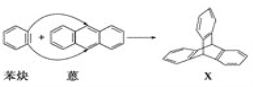
(1)蒽与X都属于___(填字母)。
a.饱和烃 b.不饱和烃
(2)苯炔的分子式为___,苯炔不具有的性质是___(填字母)。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(3)下列属于苯的同系物的是___(填字母,下同)。
A.![]() B.
B.![]()
C.![]() D.
D.![]()
(4)下列物质中,能发生加成反应,也能发生取代反应,同时能使溴水因加成反应而褪色,还能使酸性高锰酸钾溶液褪色的是___。
A.![]() B.C6H14 C.
B.C6H14 C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)镁原子由1s22s22p63s2→1s22s22p63p2时原子释放能量,由基态转化成激发态____。
(2)价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素______。
(3)凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键______。
(4)24Cr原子的电子排布式是1s22s22p63s23p63d44s2______。
(5) 金属铜属于六方最密堆积结构,金属镁属于面心立方最密堆积结构______。
(6)氯化钠晶体中,每个Na+周围距离相等的Na+共有12个______。
(7)金刚石为网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子______。
(8) 所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同______。
(9)干冰晶体中,每个CO2分子周围紧邻12个CO2分子______。
(10) 模型中的小黑点表示电子在原子核外出现的概率密度的形象描述______。
模型中的小黑点表示电子在原子核外出现的概率密度的形象描述______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com