
����Ŀ��As2O3��ҽҩ�����ӵ���������ҪӦ�ã�ij����Ԫ�أ�As���Ĺ�ҵ��ˮ����ͼ1����ת��Ϊ��As2O3 �� 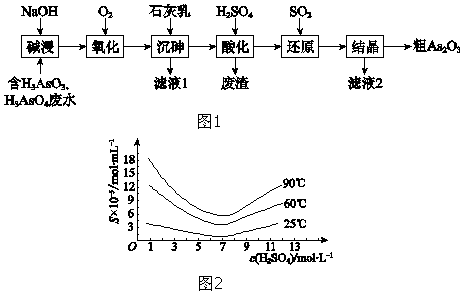
��1�����������Ŀ���ǽ���ˮ�е�H3AsO3��H3AsO4ת��Ϊ�Σ�H3AsO4ת��ΪNa3AsO4��Ӧ�Ļ�ѧ����ʽ�� ��
��2����������ʱ��1mol AsO33��ת��ΪAsO43��������ҪO2mol��
��3�������顱�ǽ���Ԫ��ת��ΪCa5��AsO4��3OH��������������Ҫ��Ӧ�У� a��Ca��OH��2��s��Ca2+��aq��+2OH����aq����H��0
b��5Ca2++OH��+3AsO43��Ca5��AsO4��3OH��H��0
�о������������顱������¶���85�森
�û�ѧƽ��ԭ�������¶ȸ���85������¶����߳������½���ԭ���� ��
��4������ԭ��������H3AsO4ת��ΪH3AsO3 �� ��Ӧ�Ļ�ѧ����ʽ�� ��
��5������ԭ���������Һ��H3AsO3�ֽ�ΪAs2O3 �� ͬʱ�ᾧ�õ���As2O3 �� As2O3�ڲ�ͬ�¶ȺͲ�ͬŨ�������е��ܽ�ȣ�S��������ͼ2��ʾ��Ϊ����ߴ�As2O3�ij����ʣ����ᾧ�����̽��еIJ����� ��
��6������˵���У���ȷ����������ĸ���� a����As2O3�к���CaSO4
b����ҵ�����У���Һ2��ѭ��ʹ�ã������Ļ�����
c��ͨ���ȡ����顱���ữ����˳���Դﵽ������Ԫ�ص�Ŀ�ģ�
���𰸡�
��1��H3AsO4+3NaOH�TNa3AsO4+3H2O
��2��0.5
��3���¶�����,��Ӧaƽ�������ƶ�,c��Ca2+���½�,��Ӧbƽ�������ƶ�,Ca5��AsO4��3OH�������½�
��4��H3AsO4+H2O+SO2�TH3AsO3+H2SO4
��5��������Ũ��ԼΪ7mol?L��1,��ȴ��25��,����
��6��abc
���������⣺��1��H3AsO4���������Ʒ�Ӧת��ΪNa3AsO4��Ӧ�Ļ�ѧ����ʽH3AsO4+3NaOH�TNa3AsO4+3H2O��
���Դ��ǣ�H3AsO4+3NaOH�TNa3AsO4+3H2O����2����������ʱ��AsO33��ת��ΪAsO43����AsԪ����+3�����ߵ�+5�ۣ�ת��2�����ӣ���1mol AsO33��ת��ΪAsO43��ת�Ƶ���2mol��������0�۽�����2�ۣ���Ҫ0.5mol��
���Դ��ǣ�0.5����3�������顱�ǽ���Ԫ��ת��ΪCa5��AsO4��3OH��������������Ҫ��Ӧ�У�a��Ca��OH��2��s��Ca2+��aq��+2OH����aq����H��0��b��5Ca2++OH��+3AsO43��Ca5��AsO4��3OH��H��0���¶����߸���85���Ӧaƽ�������ƶ���c��Ca2+���½�����Ӧbƽ�������ƶ���Ca5��AsO4��3OH�������½���
���Դ��ǣ��¶����ߣ���Ӧaƽ�������ƶ���c��Ca2+���½�����Ӧbƽ�������ƶ���Ca5��AsO4��3OH�������½�����4������ԭ�������ж�������H3AsO4��ԭΪH3AsO3�������������������ᣬ��ӦΪ��H3AsO4+H2O+SO2�TH3AsO3+H2SO4��
���Դ��ǣ�H3AsO4+H2O+SO2�TH3AsO3+H2SO4����5����ͼ2��֪������Ũ��ԼΪ7 molL��1��25��ʱAs2O3�ij�����������ڷ��룬��Ϊ����ߴ�As2O3�ij����ʣ�������Ũ��ԼΪ7 molL��1����ȴ��25�棬���ˣ�
���Դ��ǣ�������Ũ��ԼΪ7 molL��1����ȴ��25�棬���ˣ���6��a��������δ��ֳ�ȥ����As2O3�к���CaSO4����ȷ��
b����Һ2Ϊ���ᣬ��ѭ��ʹ�ã������Ļ����ʣ���ȷ��
c��ͨ���ȡ����顱���ữ����˳���Դﵽ������Ԫ�ص�Ŀ�ģ���ȷ��
���Դ��ǣ�abc��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʳ��ڷ����ڿ����У����ʹ�����û����������ԭ��Ӧ����
A. Ư�� B. Na2O C. Na D. Na2O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�¶��£����淴ӦmA��g��+nB��g��pC��g��+qD��g������H��0��ƽ�ⳣ��ΪK������˵����ȷ���ǣ� ��
A.����A������ƽ�������ƶ����ﵽ��ƽ��ʱKֵ����
B.�����¶ȣ�Kֵ����
C.KԽ��˵���÷�Ӧ�Ľ��г̶�Խ��
D.�÷�Ӧ��K= ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˳�ȥMgCl2������Һ�е�Fe3+ �� ���ڼ��Ƚ���������¼���һ���Լ����˺��ټ������������ᣬ�����Լ��ǣ� ��
A.NH3H2O
B.NaOH
C.Na2CO3
D.MgCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��a mol FeS��b mol FeOͶ�뵽V L��c mol��L��1��������Һ�г�ַ�Ӧ������NO���壬���ó�����Һ�ɷֿɿ�����Fe(NO3)3��H2SO4�Ļ��Һ����Ӧ��δ����ԭ���������Ϊ
��(a+b)��63 g ��(a+b)��189 g �� (Vc-![]() ) mol ��
) mol ��![]() mol
mol
A. �٢� B. �ڢ� C. �٢� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�Ԫ�ص�ԭ�ӻ����ӣ������Ӳ㶼�ﵽ�ȶ��ṹ���ǣ� ��
A.He��Ne��Ar��CaB.Be��B��C��Si
C.F��Cl��S��OD.Na+��F-��Cl-��Al3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ�����ķ����У���ʾ��ԭ�������ӷ���ʽ����ȷ����( )
A.������������������������Al3++3H2O ![]() Al(OH)3+3H+
Al(OH)3+3H+
B.�кͷ����ù���CO2�кͼ��Է�ˮ��CO2+2OH-=CO32-
C.����������Na2S������Hg2+��ˮ��Hg2++S2-=HgS��
D.������ԭ������FeSO4�����Է�ˮ��Cr2O72����ԭΪCr3+��Cr2O72��+6Fe2++14H+=2Cr3++6Fe3++7H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������Ҫ0.2molL��1��CuSO4��Һ950mL������ʱӦѡ�õ�����ƿ�Ĺ��ͳ�ȡ�������壨CuSO45H2O��Է�������Ϊ250���������ֱ��ǣ�������
A. 1000mL 50.0g B. 950mL 47.5g
C. 950mL 30.4g D. 1000mL 32.0g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����Ǧ�����е�Ǧ������Na2CO3��NaHCO3��Һ����Ǧ�ࣨ��Ҫ�ɷ�PbSO4�����PbCO3��PbSO4(s) + CO32-(aq) ![]() PbCO3(s) + SO42-(aq) K = 2.2��105�� �������õ���PbCO3���պ���PbO��PbO�پ�һ��ת��ΪPb������˵����ȷ����( )
PbCO3(s) + SO42-(aq) K = 2.2��105�� �������õ���PbCO3���պ���PbO��PbO�پ�һ��ת��ΪPb������˵����ȷ����( )
A.PbSO4���ܽ��С��PbCO3
B.����PbSO4��Na2CO3��NaHCO3��Һ��pH����
C.���õ��������Ũ�ȵ�Na2CO3��NaHCO3��Һ�ֱ���PbSO4 �� Na2CO3��Һ�е�PbSO4ת���ʽϴ�
D.���������漰һ�����ֽⷴӦ������������ԭ��Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com