
| A�� | ��¯ˮ���е�CaSO4������̼������Һ���ݿ�ת��ΪCaCO3 | |
| B�� | �����£��ں���Ag+��Cl-����Һ�У�Ag+��Cl-Ũ��֮���Ǹ����� | |
| C�� | ������ﵽ����ƽ��ı�ij��������ƽ��������Ӧ�����ƶ�������Һ�ĵ�������һ����ǿ | |
| D�� | ��Ũ��Ϊ0.1 mol/L��HF��Һ��ˮ����ϡ�ͣ���Һ$\frac{c��{F}^{-}��}{c��{H}^{+}��}$ʼ�ձ������� |
���� A�����ݳ���ת�������ݷ����жϣ�
B�������±���AgCl��Һ�е�Ag+��Cl-Ũ��֮���Ǹ�������
C����������������Ũ�ȳ����ȣ�
D������ϡ�͵IJ��Ͻ��У�c��H+������С��10-7mol•L-1��c��F-�����ϼ�С�����ֵ��С��
��� �⣺A������ƺ�̼��������Ӻ������ӱ���ͬ����CaCO3���ܶȻ�������CaSO4С�����Թ�¯ˮ���е�CaSO4������̼������Һ���ݿ�ת��ΪCaCO3���ټ����ᣬˮ���ܽ⣬�����˳���ת������A��ȷ��
B�������±���AgCl��Һ�е�Ag+��Cl-Ũ��֮���Ǹ������������Һ�����ͣ���Ag+��Cl-Ũ��֮��������Ũ���йأ����dz�������B����
C����Ϊ��������������Ũ�ȳ����ȣ����Ե�����ﵽ����ƽ���ˮϡ�͵���ƽ��������Ӧ�����ƶ�������Һ�ĵ���������������C����
D����ϡ��ʱһ��ʱ��������������H+��F-����Һ�������ͬ�����������ӵ�Ũ�ȵı�ֵ���䣬������ϡ�͵IJ��Ͻ��У�c��H+������С��10-7mol•L-1��c��F-�����ϼ�С�����ֵ��С����D����
��ѡA��
���� ���⿼���˳�����ת�����ܶȻ���������ʵĵ���ƽ���ƶ��ȣ����ڷ�Ӧԭ����Ӧ�õĿ��飬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ȼҩ�����β�������ҩ���ж������� | |
| B�� | ��ù���н�����ʹ������ | |
| C�� | ��˾ƥ��������Ҫ�Ŀ����� | |
| D�� | ����ҩ����ռ��������˶����Ե�ҩ���Լ���ҩ�ԣ����õ�ҽԺ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���ܵ���� | Mg��OH��2 | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| �ܽ��/g | 9��10-4 | 1.7��10-6 | 1.5��10-4 | 3.0��10-9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��Ag+�� | B�� | $\frac{c��C{l}^{-}��}{c��B{r}^{-}��}$ | C�� | c��Cl-�� | D�� | $\frac{c��A{g}^{+}��•c��B{r}^{-}��}{c��C{l}^{-}��}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��1��ͬһ���ʴ�����̬����ֵ���Һ̬����ֵ��֮����̬����ֵ��С����ͬ��ͬѹ�£�һ����Ӧ�����������������ڷ�Ӧ�����������Ϳɴ�����Ϊ�÷�Ӧ���ر�Ϊ0��ij��ѧ��ȤС�飬ר���о�������Ԫ�ؼ���ijЩ��ѧ��IJ������ʣ������������£�
��1��ͬһ���ʴ�����̬����ֵ���Һ̬����ֵ��֮����̬����ֵ��С����ͬ��ͬѹ�£�һ����Ӧ�����������������ڷ�Ӧ�����������Ϳɴ�����Ϊ�÷�Ӧ���ر�Ϊ0��ij��ѧ��ȤС�飬ר���о�������Ԫ�ؼ���ijЩ��ѧ��IJ������ʣ������������£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | PH=10��Mg��OH��2��ҺC��Mg2+��=10-8 mol•L-1 ����֪Mg��OH��2KSP=1��10-16�� | |
| B�� | ��֪AgClKSP=1.8��10-10��Ag2CrO4KSP=1.2��10-12��AgCl���ܽ��һ����Ag2CrO4�� | |
| C�� | �ڱ���AgCl��Һ�м���NaI���岻�ᷢ���仯 | |
| D�� | Fe3+��������Һ��һ����������Fe��OH��3���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
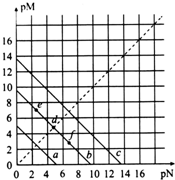 ��֪��T��ʱ��Ksp��CaSO4��=4.90��10-5��Ksp��CaCO3��=2.8��10-9��Ksp��PbCO3��=8.4��10-14�������εij����ܽ�ƽ��������ͼ��ʾ��pM=-lgc�������ӣ���pN=-lgc�������ӣ�������˵����ȷ���ǣ�������
��֪��T��ʱ��Ksp��CaSO4��=4.90��10-5��Ksp��CaCO3��=2.8��10-9��Ksp��PbCO3��=8.4��10-14�������εij����ܽ�ƽ��������ͼ��ʾ��pM=-lgc�������ӣ���pN=-lgc�������ӣ�������˵����ȷ���ǣ�������| A�� | a�ߴ�������PbCO3 | |
| B�� | T��ʱ����10 mLˮ�м���CaCO3��PbCO3�����߾����ͣ���Һ��c��Ca2+����c��Pb2+��=3��10-5 | |
| C�� | T��ʱ����CaSO4�����м���1 mol/L��Na2CO3��Һ��CaSO4������ת��ΪCaCO3���� | |
| D�� | T��ʱ����CaCO3����Һ�м���NH4Cl���壬��ʹͼ����d����f��ת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | +5 | B�� | +4 | C�� | +3 | D�� | +2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com