
【题目】在体积为1L的密闭容器中(体积不变)充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是( )
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是( )

A.进行到3分钟时,正反应速率和逆反应速率相等
B.10分钟后容器中各物质浓度不再改变
C.达到平衡后,升高温度,正反应速率增大、逆反应速率减小
D.10min内用H2的浓度变化表示的平均反应速率为0.075mol/(L·s)
【答案】B
【解析】
A. 正反应速率和逆反应速率相等,是指相同时间内物质浓度变化量相同,而根据图象可知进行到3分钟时,CO2和CH3OH的浓度相同,不能判断浓度变化量是否相同,故A错误;
B. 由图像知 10分钟后,达到平衡状态,容器中各物质浓度不再改变,故B正确;
C. 升高温度正逆反应速率均加快,故C错误;
D. 由图可知,10min到达平衡时二氧化碳的浓度变化量为1mol/L0.25mol/L=0.75mol/L,所以v(CO2)=0.75mol/L/10min=0.075mol/(Lmin),速率之比等于化学计量数之比,所以v(H2)=3v(CO2)=3×0.075mol/(Lmin)=0.225mol/(Lmin)=0.00375mol/(Ls),故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】已知在25℃,101kPa下,1gC8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.4kJ热量。表示上述反应的热化学方程式正确的是( )
A.C8H18(l)+![]() O2(g)=8CO2(g)+9H2O(g) △H=-48.4kJ·mol-1
O2(g)=8CO2(g)+9H2O(g) △H=-48.4kJ·mol-1
B.C8H18(l)+![]() O2(g)=8CO2(g)+9H2O(l) △H=-5517.6kJ·mol-1
O2(g)=8CO2(g)+9H2O(l) △H=-5517.6kJ·mol-1
C.C8H18(l)+![]() O2(g)=8CO2(g)+9H2O(l) △H=+5517.6kJ·mol-1
O2(g)=8CO2(g)+9H2O(l) △H=+5517.6kJ·mol-1
D.C8H18(l)+![]() O2(g)=8CO2(g)+9H2O(l) △H=-48.4kJ·mol-1
O2(g)=8CO2(g)+9H2O(l) △H=-48.4kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是
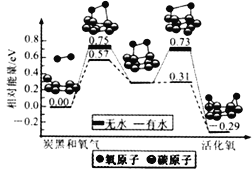
A. 氧分子的活化包括O-O键的断裂与C-O键的生成
B. 每活化一个氧分子放出0.29eV的能量
C. 水可使氧分子活化反应的活化能降低0.42eV
D. 炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学工作者研发了一种 SUNCAT的系统,借助锂循环可持续合成氨,其原理如下图所示。下列说法不正确的是
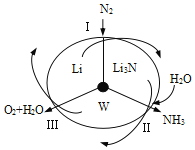
A. 过程I得到的Li3N中N元素为—3价
B. 过程Ⅱ生成W的反应为Li3N+3H2O===3LiOH+NH3↑
C. 过程Ⅲ中能量的转化形式为化学能转化为电能
D. 过程Ⅲ涉及的反应为4OH--4e-=O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定法是化学上常用的定量分析的方法,滴定的方法有酸碱中和滴定、氧化还原滴定、沉淀滴定、络合滴定等。
Ⅰ.甲化学兴趣小组取20.00 mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用0.200 0 mol·L-1的标准NaOH溶液进行滴定,重复上述滴定操作3次,并记录数据。
(1)滴定时边滴边摇动锥形瓶,眼睛应观察________。(填标号)
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(2)判断滴定终点的现象是_________________。
(3)根据表中数据,计算待测盐酸溶液的浓度为________ mol·L-1。
滴定次数 | 待测液体积(mL) | 标准NaOH溶液读数记录(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 4.00 | 24.00 |
第三次 | 20.00 | 2.00 | 24.10 |
Ⅱ.乙化学兴趣小组利用氧化还原反应滴定,测定了某工厂废水中游离态氯的含量。实验如下:
①取水样10.0 mL于锥形瓶中,加入10.0 mL的KI溶液(足量),滴入指示剂2~3滴。
②将自己配制的0.01 mol·L-1标准Na2S2O3溶液装入滴定管中,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为I2+2Na2S2O3=2NaI+Na2S4O6,试回答下列问题:
(4)步骤①发生的化学反应方程式为__________;加入的指示剂是____________。
(5)步骤②应使用________式滴定管。
(6)氯的所测浓度比实际浓度会偏大,造成误差的原因可能是________。(填标号)
A.配制标准Na2S2O3溶液定容时,加水超过刻度线
B.锥形瓶水洗后直接装待测水样
C.装标准Na2S2O3溶液的滴定管水洗后没有润洗
D.滴定到达终点时,俯视读出滴定管读数
E.滴定前尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是重要的有机合成中间体,H为高分子化合物,其合成路线如图所示:
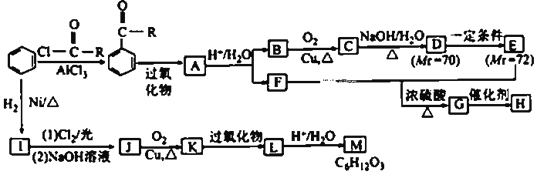
已知:①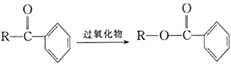 (R为烃基);
(R为烃基);
②2R-CH2CHO![]()
![]() 。
。
请回答下列问题:
(1)E中所含官能团的名称为____________。H的结构简式为____________。
(2)C→D涉及的反应类型有____________________________。
(3)A→B+F的化学方程式为___________________________________。
(4)D与银氨溶液反应的化学方程式为___________。
(5)符合下列条件的M的同分异构体有____________种(不考虑立体异构)。
①官能团种类和数目与M相同
②分子中含有1个-CH3和1个-CH2CH2-
③不含-CH2CH2CH2-
(6)请结合所学知识和上述信息,写出以苯甲醛和一氯乙烷为原料(无机试剂任选),制备苄基乙醛(![]() )的合成路线:________________________。
)的合成路线:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25℃时,0.1mol L-1NaOH溶液中,Kw=__;pH=__。
(2)氯化铁水溶液呈___(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):__。实验室在配制氯化铁溶液时,常将氯化铁固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,是为了___(填“促进”、“抑制”)氯化铁水解。
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈__(填“酸性”,“中性”或“碱性”),溶液中c(Na+ )___c(CH3COO-)(填“>”,“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向20.00mL0.100molL-1的氨水和醋酸铵溶液中分别滴加0.100molL-1的盐酸溶液,溶液pH随加入盐酸体积的变化如图所示。下列说法不正确的是( )
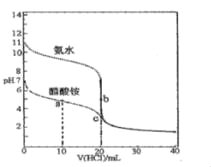
A.25℃时,Kb(NH3H2O)=Ka(CH3COOH)≈10-5
B.b点溶液中水的电离程度比c点溶液中的大
C.在c点的溶液中:c(Cl﹣)>c(CH3COOH)>c(NH4+)>c(OH﹣)
D.在a点的溶液中:c(NH4+)+2c(H+)═2c(CH3COO-)+c(NH3H2O)+2c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1 mol·L-1,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100 mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是

A. Ka(HA)=1×10-6
B. b点c(B+)=c(A-)=c(OH-)=c(H+)
C. a→c过程中水的电离程度始终增大
D. c点时,c(A-)/[c(OH-)c(HA)]随温度升高而减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com