



 ,说明X原子失去最外层的a个电子变成+2价的阳离子,所以X为Ca,Y为Cl;D、E原子的最外层电子数是其电子层数的2倍,则其为He或C或S或Kr,又因D与Y相邻,则D为S,He、Kr与D不能形成分子,则E为C,C与S形成的分子为CS2,然后根据问题解答.
,说明X原子失去最外层的a个电子变成+2价的阳离子,所以X为Ca,Y为Cl;D、E原子的最外层电子数是其电子层数的2倍,则其为He或C或S或Kr,又因D与Y相邻,则D为S,He、Kr与D不能形成分子,则E为C,C与S形成的分子为CS2,然后根据问题解答. ,故A错误;
,故A错误;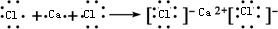 ,故D正确;
,故D正确;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:




查看答案和解析>>
科目:高中化学 来源: 题型:





查看答案和解析>>
科目:高中化学 来源:2013届江西省高一下学期第六次段考化学试卷 题型:填空题
(10分) 在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式是 ;X与氢元素形成的化合物的电子式是 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是 ;D与E能形成一种非极性分子,该分子的结构式为 ;D所在族元素的氢化物中,沸点最低的氢化物的化学式是 。
(3)元素W与Y同周期,其单质是一种良好的半导体材料;元素Z的单质分子Z2中由3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是 。
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,此反应的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com