
|
实验中需用2.0 mol/L的Na2CO3溶液950 mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别为 | |
| [ ] | |
A. |
1000 mL,212 g |
B. |
950 mL,201.4 g |
C. |
100 mL,21.2 g |
D. |
500 mL,100.7 g |
科目:高中化学 来源: 题型:

| 1 |
| 2 |
| 1 |
| 2 |
| △H2+△H2-△H3 |
| 3 |
| △H2+△H2-△H3 |
| 3 |
| c(H2O) |
| c(H2) |
| c(H2O) |
| c(H2) |
| 实验 编号 |
催化剂 | 反应时间和m(O2)/g | |||||
| 10s | 20s | 30s | 40s | 50s | 60s | ||
| 1 | α-Fe2O3 | 0.055 | 0.215 | 0.290 | 0.310 | 0.320 | 0.320 |
| 2 | γ-Fe2O3 | 0.053 | 0.220 | 0.291 | 0.310 | 0.320 | 0.320 |
| 3 | MnO2 | 0.065 | 0.270 | 0.300 | 0.320 | 0.320 | 0.320 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
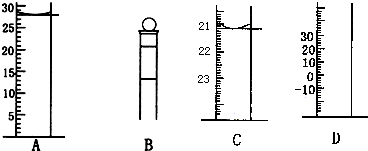
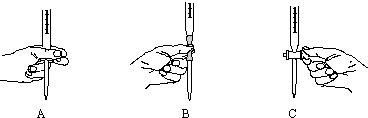
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
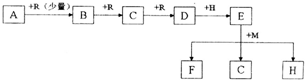
| ||
| ||

| ||
| ||
| 20V |
| 7 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省荆州市毕业班质量检查(一)化学试卷(解析版) 题型:填空题
铁黄是一种重要的颜料,化学式为Fe2O3·xH2 O,广泛用于涂料、橡胶、塑料、文教用品等工业。实验室模拟工业利用硫酸渣(含FeZ 0。及少量的CaO, Mg0等)和黄铁矿粉
(主要成分为FeS2)制备铁黄的流程如下:
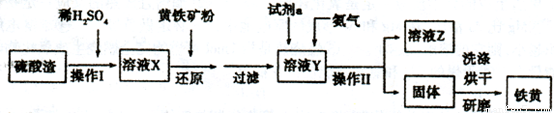
(1)操作I与操作II中都用到玻璃棒,玻璃棒在两种操作中的作用分别是_ 、
(2)试剂a最好选用_ (供选择使用的有:铝粉、空气、浓HNO3 );其作用是_ 。
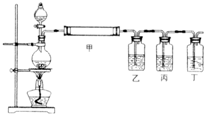
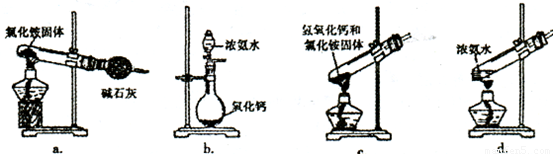
(3)上述步骤中需用到氨气。下列装置可用于实验室制氨气的是_ _(填序号)。
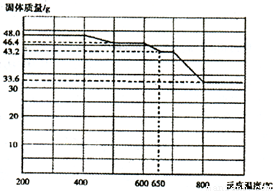
(4)查阅资料知,在不同温度下Fe2 O3被CO还原,产物可能为Fe3 O4 、FeO或Fe,固体质量与反应温度的关系如右图所示。根据图象推断670℃时Fe2 O3还原产物的化学式为M,并设计一个简单的实验,证明该还原产物的成分(依次填写每步操作中所加试剂的化学式、现象和结论)。仪器自选。可供选择的试剂:稀H2SO4、稀盐酸、H2 O2溶液、NaOH溶液、KSCN溶液。
|
加入试剂 |
现象 |
结论 |
|
|
|
则还原产物为 |
|
|
|
|
|
|
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com