
【题目】二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向。
(1)CO2的电子式是 ,所含化学键的类型是 。
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
①写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式 。
②一定条件下,上述合成二甲醚的的反应达到平衡状态后,若改变反应的某个条件,下列变化能说明平衡一定向正反应方向移动的是(只有一个选项符合题意) (填字母代号)。
a.逆反应速率先增大后减小
b.H2的转化率增大
c.CO2的体积百分含量减小
d.容器中c(H2)/c(CO2)的值减小
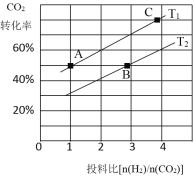
③在某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的平衡转化率如右图所示。T1温度下,将6 molCO2和12 molH2充入2 L的密闭容器中,5 min后反应达到平衡状态,则0~5 min内的平均反应速率v(CH3OCH3)= ;KA、KB 、KC三者之间的大小关系为 。
(3)CO2溶于水形成H2CO3。已知常温下H2CO3的电离平衡常数K1=4.4×10-7,K2=4.7×10-11,NH3·H2O的电离平衡常数K=1.75×10-5。常温下,用氨水吸收CO2可得到NH4HCO3溶液,NH4HCO3溶液显 ;(填“酸性”、“中性”或“碱性”);请计算反应NH4++HCO3-+H2O![]() NH3·H2O+H2CO3的平衡常数K= 。
NH3·H2O+H2CO3的平衡常数K= 。
【答案】(1)![]() ; 共价键(或极性键);
; 共价键(或极性键);
(2)①2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) △H=-122.7 kJ·mol-1;②b;③0.18 mol·L-1·min-1; KA = KC>KB;
CH3OCH3(g)+3H2O(g) △H=-122.7 kJ·mol-1;②b;③0.18 mol·L-1·min-1; KA = KC>KB;
(3)碱性;1.3×10-3;
【解析】
试题分析:(1)因为CO2为共价化合物,则电子式为![]() ,所含化学键为共价键,故答案为:
,所含化学键为共价键,故答案为:![]() ;共价键;
;共价键;
(2)①CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H1=-49.1kJmol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H2=-24.5kJmol-1
①根据盖斯定律①×2+②,则CO2(g)加H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式为2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-122.7 kJmol-1;故答案为:2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-122.7 kJmol-1;
②a.逆反应速率先增大后减小,说明平衡向逆反应方向移动,故不选;b.H2的转化率增大,说明平衡向正反应方向移动,故选;c.CO2的体积百分含量减小,可能为减小二氧化碳的量使平衡向逆反应方向移动,故不选;d.容器中c(H2)/c(CO2)的值减小,可能为减小氢气的量使平衡向逆反应方向移动,故不选;故选:b;
③T1温度下,将6molCO2和12molH2充入2L的密闭容器中,由图象可知,5min后反应达到平衡状态时二氧化碳转化率为60%,则生成CH3OCH3为6mol×60%×![]() =1.8mol,所以平均反应速率v(CH3OCH3)=
=1.8mol,所以平均反应速率v(CH3OCH3)=![]() =
=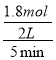 0.18 mol.L-1min-1;又平衡常数仅与温度有关,所以KA=KC,又根据图象在相同投料比时T1温度下二氧化碳转化率大,所以T1温度下较T2温度下反应向正反应方向移动,则KA=KC>KB,故答案为:0.18 mol.L-1min-1;KA=KC>KB;
0.18 mol.L-1min-1;又平衡常数仅与温度有关,所以KA=KC,又根据图象在相同投料比时T1温度下二氧化碳转化率大,所以T1温度下较T2温度下反应向正反应方向移动,则KA=KC>KB,故答案为:0.18 mol.L-1min-1;KA=KC>KB;
(3)根据盐类水解规律,已知NH3.H2O的电离平衡常数K=1.75×10-5,H2CO3的电离平衡常数K1=4.4×10-7,K2=4.7×10-11,所以碳酸氢根的水解程度更大,所以NH4HCO3显碱性;反应NH4++HCO3-+H2O═NH3.H2O+H2CO3的平衡常数K= =
=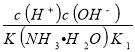 =
=![]() =1.3×10-3;故答案为:碱性;1.3×10-3。
=1.3×10-3;故答案为:碱性;1.3×10-3。


科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
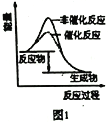


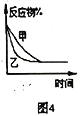
A. 图1表示分别在有、无催化剂的情况下某吸热反应过程中的能量变化
B. 图2表示常温下,等量锌粉与足量的等浓度的盐酸反应(滴加CuSO4溶液的为虚线)
C. 图3表示mg冰醋酸加水稀释过程中溶液导电能力的变化,其中醋酸的电离度c>b>a
D. 图4表压强对合成氨反应的影响,乙的压强大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的金属Na、Mg、Al分别与100 mL 2 mol·L-1的盐酸反应,实验测得生成气体的体积V (已折合为标准状况)与时间t的关系如图所示,则下列说法错误的是
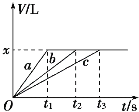
A. x=2.24 B. 曲线b为Mg与盐酸反应的图象
C. 反应时,Na、Mg、Al均过量 D. 钠的物质的量为0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向80mL浓硫酸中加入56g铜片,加热一段时间后,至不再反应为止,计算:
(1)实验测得反应中共有13.44L标准状况下的SO2生成,被还原的硫酸的物质的量为_____mol,反应中转移的电子有_____mol。
(2)将反应后的混合物加水稀释到100mL并除去不溶物,加入足量锌粉放出标准状况下5.376L氢气,则原浓硫酸的物质的量浓度为_____,反应的Zn的质量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是(NA为阿伏加德罗常数)
A. 标准状况下,1mol SiO2所占体积约为22.4L
B. 相同质量的O2和O3含有相同数目的氧原子
C. 常温下,11.2L CO2含有分子数为0.5NA
D. 2.4g金属镁变成镁离子时失去电子的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 漂白粉溶液漂白的原理是与空气中的CO2反应生成次氯酸
B. 84消毒液的主要成分是次氯酸钠
C. 金属钠保存在煤油中
D. 久置氯水酸性会减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.58kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g)![]() CH3OH(g) △H3=-90.77kJ·mol-1
CH3OH(g) △H3=-90.77kJ·mol-1
回答下列问题:
(1)反应Ⅱ的△H2=______________。
(2)反应Ⅲ能够自发进行的条件是__ (填“较低温度”、“ 较高温度”或“任何温度”)
(3)恒温,恒容密闭容器中,对于反应Ⅰ,下列说法中能说明该反应达到化学平衡状态的是________。
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1
D.甲醇的百分含量不再变化
(4)对于反应Ⅰ,不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法不正确的是____。
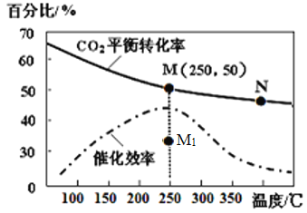
A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
B.温度低于250℃时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)若在1L密闭容器中充入3molH2和1molCO2发生反应Ⅰ,250℃时反应的平衡常数K=__________;若要进一步提高甲醇积分数。可采取的措施有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①KClO3 + HCl-----Cl2↑+ KCl + H2O
②Cl2+2KI═2KCl+I2
③I2+5Cl2+6H2O═2HIO3+10HCl
回答下列问题:
(1)反应③中氧化产物是__________(填化学式)
(2)配平反应①并用单线桥法表示该反应中电子转移的方向和数目___KClO3 + ___HCl=_____Cl2↑+____ KCl + ____H2O,______________。
(3)下列说法正确的是______。
A. 反应③中氧化剂和还原剂的物质的量之比为1:5
B.结合反应②③,若将Cl2通入含有淀粉的KI溶液中,可能会观察到先变蓝后褪色
C.还原性由强到弱顺序:Cl-> I-
D.氧化性由强到弱顺序:KClO3>Cl2>I2
(4)实验室用反应①可以制取Cl2,若反应消耗24.5g KClO3,则至少需用________mL 6mol/LNaOH溶液吸收产生的氯气。写出吸收氯气的离子方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A. 盐酸与氨水反应:H++OH-=H2O
B. 铜粉与稀硝酸的反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
C. Cl2与H2O的反应:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
D. 碳酸钙溶液与足量稀盐酸的反应:CO32-+2H+=H2O+CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com