
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.0.2molAl与足量NaOH溶液反应,生成的H2分子数为0.3NA
B.常温下,1LpH=1的盐酸溶液,由水电离的H+离子数目为0.1NA
C.铅蓄电池中,当正极增加9.6g时,电路中通过的电子数目为0.2NA
D.11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4 反应中,6 mol CuSO4能氧化白磷的分子数为1.1NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
设nA为阿伏伽德罗常数的数值,下列说法正确的是
A. 23g Na 与足量H2O反应完全后可生成nA个H2分子
B.1 molCu和足量热浓硫酸反应可生成nA个SO3分子
molCu和足量热浓硫酸反应可生成nA个SO3分子
C.标准状况下,22.4L N2和H2混合气中含nA个原子
D.3mol单质Fe完全转变为Fe3O4,失去8nA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
进行化学实验时应强化安全意识。下列做法正确的是:
A.金属钠着火时使用泡沫灭火器灭火
B.用试管加热碳酸氢钠固体时使试管口竖直向上
C.浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗
D.制备乙烯时向乙醇和浓硫酸的混合液中加入碎瓷片
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案设计中,不能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 验证乙烯与溴发生加成反应 | 乙烯通入溴水中,测定反应前后溶液pH |
| B | 检验氯化铁溶液中是否含FeCl2 | 向氯化铁溶液中滴加铁氰化钾溶液 |
| C | 检验乙酸中是否混有乙醇 | 取样液于试管,加入一绿豆颗粒大的钠粒 |
| D | 验证Ksp(AgI)<Ksp(AgCl) | 向含等物质的量NaCl、KI的混合液中滴加AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中粒子的物质的量浓度关系正确的是
A.NaH2PO4酸性溶液中:
c(Na+)>c(H2PO4-)>c(H3PO4)>c(HPO42-)
B.0.1mol·L-1CH3COONa溶液与0.1mol·L-1CH3COOH溶液等体积混合(pH<7)
c(CH3COOH) >c(Na+)>c(CH3COO-)>c(H+)
C.0.1mol·L-1(NH4)2SO4溶液与0.1mol·L-1NH3·H2O溶液等体积混合:
c(NH4+)+c(H+)=2c(SO42-)+c(OH-)
D.0.1mol·L-1Na2CO3溶液与0.2mol·L-1NaHCO3溶液等体积混合:
 c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学设计原电池装置如图所示。下列说法正确的是( )
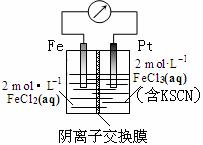 A.电子由铁极经溶液向铂极迁移
A.电子由铁极经溶液向铂极迁移
B.放电过程中交换膜右侧溶液颜色逐渐变浅
C.正极的电极反应式为Fe3++3e=Fe
D.若转移2mol e,交换膜右侧溶液中约减少3 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组拟制备氯气并验证其一系列性质。
Ⅰ.【查阅资料】
①当溴水浓度较小时,溶液颜色与氯水相似也呈黄色。
②硫代硫酸钠溶液在工业上可作为脱氯剂 。
Ⅱ.【性质验证】
实验装置如图所示(省略夹持装置)
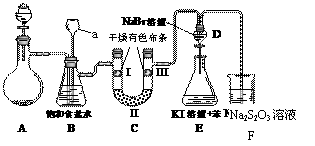

实验步骤:
(1)检查装置气密性,按图示加入试剂。仪器a的名称是 ;装置CⅡ处加的试剂可以是 (选填下列字母编号)。
A.碱石灰 B.硅胶 C.浓硫酸 D.无水氯化钙
(2)装置B的作用有 。
(3)写出装置F中相应的离子反应方程式: 。
Ⅲ.【探究与反思】
 (1)上图中设计装置D、E的目的是比较氯、溴、碘的非金属性,有同学认为该设计不能达到实验目的,其理由是 。该组的同学思考后将上述D、E、F装置改为实验操作步骤如下:
(1)上图中设计装置D、E的目的是比较氯、溴、碘的非金属性,有同学认为该设计不能达到实验目的,其理由是 。该组的同学思考后将上述D、E、F装置改为实验操作步骤如下:
①打开弹簧夹,缓缓通入氯气
②当a和b中的溶液都变为黄色时,夹紧弹簧夹。
③当a中溶液由黄色变为棕色时,停止通氯气。
④___。
(2)设计步骤③的实验思想是 。
(3)步骤④的操作是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用铜和浓硫酸反应制取二氧化硫,下列有关该反应的说法错误的是
A.铜是还原剂,发生了氧化反应
B.每生成64 g SO2,转移电子的物质的量是2 mol
C.每消耗1 mol Cu,起氧化剂作用的硫酸消耗2 mol
D.在此反应中,浓硫酸表现出酸性和氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com