
| A.由②中的实验现象可推测一定含有NO2- |
| B.根据②③④可确定一定含有NO2-、CO32-、Cl-三种阴离子 |
| C.不能确定是否一定含有NO3- |
| D.由④即可确定一定不存在SO42-、SO32- |


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源:不详 题型:单选题
| A.4种 | B.5种 | C.6种 | D.7种 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H++A2-。现有下列四种溶液:
H++A2-。现有下列四种溶液: H2A+OH-
H2A+OH-查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
| B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的102倍 |
| C.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO42- |
| D.常温时,0.l mol/L HA溶液的pH>l,0.1 mol/L BOH溶液中c(OH-)/c(H+)=l012,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为:c(B+)>c(OH-)>c(H+)>c(A-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.无色溶液:K+、Al3+、NO3—、AlO2— |
| B.pH=12的溶液:K+、Cl-、SO32—、SiO32— |
| C.含0.1 mol·L-1 NO3—的溶液:H+、Fe2+、Cl-、SO42— |
| D.由水电离产生的c(H+)=1×10-12 mol·L-1的溶液:Na+、NH4+、SO42—、HCO3— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.强碱性溶液中:K+、Al3+、Cl-、SO42- |
| B.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、NO3- |
| C.含有0.1 mol·L-1 Ca2+溶液在中:Na+、K+、CO32-、Cl- |
| D.室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe2+、Mg2+、ClO-、Cl-能大量共存 |
| B.含Br-、K+、Na+、HSO3-的溶液,通入SO2后这些离子仍能大量共存 |
C.含K+、Na+、NO3-、CH3COO-的溶液中c(H+)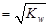 |
| D.硝酸钠和碘化钡混合溶液中,溶质离子浓度为c (Ba2+)=0.2mol/L,c(Na+)=0.2mol/L,c(NO3-)=0.3mol/L,c(I-)=0.1mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com