
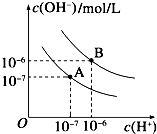
 已知水在25℃和95℃时的电离平衡曲线如下图所示:
已知水在25℃和95℃时的电离平衡曲线如下图所示:分析 (1)水的电离是吸热过程,降低温度抑制水电离,导致水中c(H+)、c(OH-)都减小;根据溶液的pH计算出溶液中氢离子、氢氧根离子浓度,再列式计算出氢氧化钠溶液和硫酸溶液的体积;
(2)先设出强酸、强碱的pH值,利用酸碱混合后溶液显中性,则n(H+)=n(OH-),然后可依据物质的量的关系来列式寻找pH的关系;
(3)水中氢离子、碱中氢氧根离子浓度越大,水的电离程度越小;恰好反应后溶液显示酸性,则反应生成了强酸弱碱盐,碱根离子水解,溶液显示酸性;
(4)根据图象判断该温度下水的离子积,然后计算出混合液中氢氧根离子浓度,再结合该温度下水的离子积计算出所带溶液中氢离子浓度及溶液的pH.
解答 解:(1)水的电离是吸热过程,升高温度,使水的电离程度增大,当温度升高时,促进水的电离,水的离子积增大,水中氢离子、氢氧根离子浓度都增大,水的pH减小,但溶液仍然呈中性;25℃时所得混合溶液的pH=7,溶液呈中性即酸碱恰好中和,即n(OH-)=n(H+),则V(NaOH)•10-5 mol•L-1=V(H2SO4)•10-4 mol•L-1,得V(NaOH):V(H2SO4)=10:1,
故答案为:A;水的电离是吸热过程,温度低时,电离程度小,c(H+)、c(OH-)小;10:1;
(2)强酸的pH=a,强碱的pH=b,由95℃时,若100体积的某强酸溶液与1体积的某强碱溶液混和后溶液呈中性,即n(H+)=n(OH-),则100×10-a=1×10b-12,102-a=10b-12,即2-a=b-12,则a+b=14,故答案为:a+b=14;
(3)在曲线A中,水的离子积为10-7×10-7=10-14,pH=2的HCl中c(H+)=10-2mol/L,pH=11的某BOH溶液中c(OH-)=10-3mol/L,因c(H+)>c(OH-),故在盐酸中水的电离受到的抑制作用比较大,即:α1小于α2;pH=2的HCl中c(H+)=10-2mol/L,pH=11的某BOH溶液中c(OH-)=10-3mol/L,如果BOH是强碱,则二者等体积混合,酸剩余,所以pH小于7,假设BOH是弱碱,则BOH的浓度会大于0.001mol/L,但是和0.01mol/L的盐酸相对浓度大小无法判断,所以此时溶液的pH无法判断,
故答案为:无法判断;如果BOH是强碱,则二者混合,酸剩余,所以pH小于7,假设BOH是弱碱,则BOH的浓度会大于0.001mol/L,但是和0.01mol/L的盐酸相对浓度大小无法判断;
(4)在曲线B中,水的离子积为:10-6×10-6=10-12,0.02mol/L的Ba(OH)2溶液中c(OH-)=0.04mol/L,NaHSO4溶液的浓度为0.02mol/L,c(H+)=0.02mol/L,当二者等体积混合后,溶液中的c(OH-)=$\frac{0.04molo/L-0.02mol/L}{2}$=0.01mol/L,则c(H+)=$\frac{1{0}^{-12}}{0.01}$=10-10mol/L,该溶液的pH=10,
故答案为:10.
点评 本题考查水的电离和酸、碱混合的pH计算问题,难度较大,注意温度不同而使水的离子积常数不同是解本题的关键.(4)为易错点,需要明确该温度下水的离子积为10-6×10-6=10-12,试题充分考查了学生的分析、理解能力及化学计算能力.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 1 mol H2O的质量为18g/mol | |
| B. | 标准状况下,1 mol任何物质体积均为22.4L | |
| C. | CH4的摩尔质量为16g | |
| D. | 6.02×1023个O2分子的质量为32g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
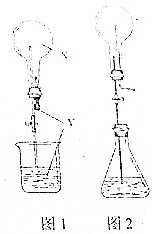 关于喷泉实验,回答下列问题:
关于喷泉实验,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10.6g | B. | 12.6g | ||
| C. | 15.9g | D. | 数据不足,无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将0.2mol•L-1氨水与0.2mol•L-1盐酸混合,c(NH3•H20)+c(NH4+)=c(Cl-) | |
| B. | 常温下NH4A溶液中的pH=6,则c(A-)-c(NH4+)=9.9×10-7mol•L-1 | |
| C. | c(NH4+)相等的NH4Cl,NH4HCO3溶液中,溶质初始浓度:c(NH4Cl)=c(NH4HCO3) | |
| D. | 将0.2molCO2缓慢通入含有0.3molNAOH的溶液中,c(CO32-)>c(HCO3-)>c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| B | ||
| A | C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com