
【题目】某溶液只含Cl![]() 、CO
、CO![]() 、SO
、SO![]() 、Na
、Na![]() 、K
、K![]() 、Mg
、Mg![]() 六种离子中的某几种。经实验:
六种离子中的某几种。经实验:
①原溶液![]() 白色沉淀;
白色沉淀;
②原溶液中加BaCl2溶液不产生沉淀;
③原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。回答下列问题:
(1)试分析原溶液中一定含有的离子是______________,一定不含有的离子是_______,可能含有的离子是______________。
(2)有的同学认为实验③可以省略,你认为是否正确(填“是”或“否”)_________,说明理由_________________________________________________________。
【答案】 Mg2+、Cl- CO32-、SO42- K+、Na+ 是 溶液必须呈电中性,有Mg2+,无CO32-、SO42-,则必然有Cl-
【解析】⑴.题目所给的六种离子中,只有Mg2+遇NaOH可以生成白色沉淀,则原溶液中一定含有Mg2+;向原溶液中加入BaCl2溶液不产生沉淀,则原溶液中一定没有CO32-和SO42-;原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解,说明原溶液中一定含有Cl-,则可能含有的离子是K+、Na+,故答案为: Mg2+、Cl-;CO32-、SO42-; K+、Na+;
⑵.根据上述分析可知,原溶液中一定有Mg2+,根据溶液电中性原则,溶液中一定含有阴离子,但根据上述判断可知原溶液中无CO32-、SO42-,则一定含有Cl-,故答案是:是;溶液必须呈电中性,有Mg2+,无CO32-、SO42-,则必然有Cl-。


科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。
已知:①亚氯酸钠(NaClO2)受热易分解。
②NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O;
③纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
以氯酸钠等为原料制备亚氯酸钠的工艺流程如下

(1)“反应1”需要鼓入空气,空气的作用是 __________________________________。
(2)“反应2”的化学方程式为_________________________________。
(3)采取“减压蒸发”而不用“常压蒸发”,原因是___________________;结晶后需要对晶体洗涤,为了减少损失,可以用_____________ 洗涤晶体。
(4)从“母液”中可回收的主要物质是_____________ 。
(5)要得到纯的亚氯酸钠晶体(NaClO2·3H2O),对粗产品必须进行的操作为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前人类已发现的非金属元素除稀有气体外,共有16种,对这16种非金属元素的相关判断:①都是主族元素,最外层电子数都大于4;②单质在反应中都只能作氧化剂;③氢化物常温下都是气态;④氧化物常温下都可以与水反应生成酸。其中不正确的有( )
A. ①② B. ①③ C. ③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原子最外层电子排布为2s22p3,则该原子
A. 核外有5个电子
B. 核外有3种能量不同的电子
C. 最外层电子占据3个轨道
D. 最外层上有3种运动状态不同的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某化学小组用实验的方法进行探究。他们只利用Cu、 Fe、 Mg和不同浓度的硫酸(0. 5 mol·L-1 、2 mol·L-1、18.4 mol·L-1)设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
实验步骤 | 现象 | 结论 |
①分别取等体积的2 mol·L-1的硫酸于三支试管中; ②__________________________________ | 反应速率Mg>Fe,Cu不反应 | 金属的性质越活泼,反应速率越快 |
(1)甲同学表中实验步骤②操作为____________________________。
(2)甲同学的实验目的是_____________________;要得出正确的实验结论,还需控制的实验条件是__________________________________________。
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。

(3)乙同学在实验中应该测定的数据是______________。
(4)乙同学完成该实验应选用的实验药品是____________________________。
该实验中不选用某浓度的硫酸,理由是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰(CN)2的结构简式为N≡C—C≡N,其化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间。下列有关反应的化学方程式不正确的是( )
A. (CN)2+H2=2HCN
B. MnO2+4HCN=Mn(CN)2+(CN)2↑+2H2O
C. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
D. 在NaBr和KCN混合液中通入少量Cl2:Cl2+2KCN=2KCl+(CN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水和重水分别跟金属钾反应,若两反应中电子转移总数相等时,下列物质的化学量相等的是 :①消耗水和重水的质量; ②同温同压下生成气体的体积;③生成气体的质量; ④参加反应的钾的质量。
A.①③ B.②④ C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。下列分析或结果错误的是
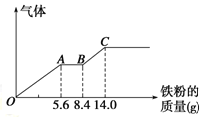
A.原混合酸中NO3-物质的量为0.1 mol
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.H2SO4浓度为2.5 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com