
【题目】如图所示,下列说法正确的是( ) 
A.甲池中阳离子向通入CH3OH一方的电极区域内移动
B.甲池通入CH3OH的电极反应式为CH3OH﹣6e﹣+2H2O═CO32﹣+8H+
C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度
D.甲池中消耗280 mL(标准状况下)O2 , 此时丙池中理论上产生1.45 g固体
【答案】D
【解析】解:A、甲池是燃料电池,在燃料电池中,通入CH3OH的电极是负极,阳离子向通入氧气一方的正极区域内移动,故A错误;B、在燃料电池中,负极是甲醇发生失电子的氧化反应,在碱性电解质下的电极反应为CH3OH﹣6e﹣+2H2O+8OH﹣=CO32﹣+8H2O,故B错误;
C、电解池乙池中,电解后生成硫酸、铜和氧气,要想复原,要加入氧化铜,故C错误;
D、甲池中根据电极反应:O2+2H2O+4e﹣=4OH﹣ , 所以消耗280mL(标准状况下0.0125mol)O2 , 则转移电子0.05mol,根据丙装置中,在阴极上是氢离子放电,减小的氢离子是0.025mol,所以镁离子和氢氧根离子之间反应生成氢氧化镁,理论上最多产生氢氧化镁质量应该是0.125×2mol×58g/mol=1.45g固体,故D正确.
故选D.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:
【题目】用 0.2 mol·L -1某金属阳离子 Rn+的盐溶液 40mL,恰好将 20 mL 0.4 mol·L -1的硫酸盐中的硫酸根离子完全沉淀,则 n 值为( )
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置:
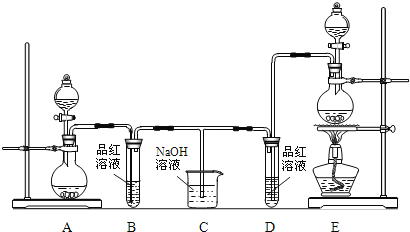
(1)实验室制备Cl2的离子方程式是_____________________________,应选用上图A、E装置中的______(填序号)制Cl2,反应中浓盐酸所表现出的性质是_________________。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是___________________________________。
(3)装置C的作用是____________________________________。
(4)甲乙两名同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性。试分析:
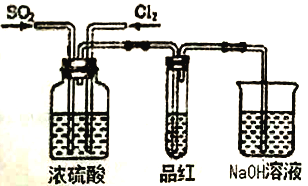
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是_____________________。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是(用相应的离子方程式作答)____________
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅,原因是_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在KCl、MgCl2、Mg(NO3)2形成的混合溶液中,c(K+)=0.1mol/L,c(Mg2+)=0.15mol/L,c(Cl﹣)=0.2mol/L,则c(NO3﹣)为( )
A.0.05 mol/L
B.0.20 mol/L
C.0.30 mol/L
D.0.40 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学的发展史上,许多科学家创建的理论对化学科学的发展起到重大的作用。有关科学家与其创建的理论对应不匹配的是( )
A.墨子:物质的分割是有条件的
B.汤姆生:葡萄干面包模型
C.德谟克利特:古典原子论
D.贝克勒尔:原子结构的行星模型
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①大豆油和氯化钠溶液 ②39%的乙醇溶液 ③硫酸钠和单质溴的水溶 液,分离以上各混合液的正确方法依次是 ( )
A. 分液、萃取、蒸馏 B. 分液、蒸馏、萃取
C. 萃取、蒸馏、分液 D. 蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的 X 置于某 10L 容积恒定的真空容器中(假设固体试样体积忽略不计),在恒定温度下使其达到分解平衡:X(s)2Y(g)+Z(g),实验测得不同温度下的分解平衡常数列于如表,下列说法中不正确的是( )
温度( | 15.0 | 25.0 | 30.0 | 35.0 |
K/(×10﹣8 mol3L﹣3) | 0.205 | 1.64 | 4.68 | 10.8 |
A.若Z的体积分数不再随时间变化时表示反应达平衡状态
B.35 ![]() 时,达平衡时,X分解了 0.03 mol
时,达平衡时,X分解了 0.03 mol
C.该反应在高温下可能自发
D.若在恒温下,压缩容器体积,再次达平衡后,n(X)比原平衡大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%浓硫酸配制0.1mol/L的稀硫酸,下列情况会使所配溶液浓度偏低的是( )
A.未冷却就转移、定容
B.容量瓶内原有少量蒸馏水
C.定容时俯视刻度线观察液面
D.定容时加多了水再用吸管吸出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com