
 ij���淴Ӧ��ij���Ϊ5L���ܱ������н��У��ڴ�0��4���Ӹ����ʵ����ı仯�����ͼ��ʾ��X��Y��Z��Ϊ���壩��
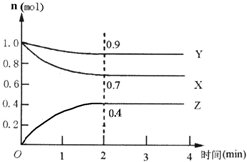
ij���淴Ӧ��ij���Ϊ5L���ܱ������н��У��ڴ�0��4���Ӹ����ʵ����ı仯�����ͼ��ʾ��X��Y��Z��Ϊ���壩������ ��1���������ʵ����ı仯�жϷ�Ӧ���������������ʵ����ı仯֮�ȵ��ڻ�ѧ������֮����д����ʽ��
��2������v=$\frac{��c}{��t}$���㷴Ӧ���ʣ�
��3�����ݵ�4����ʱ�������ʵ������䣬��Ӧ��ƽ��״̬����Ӧ����֮�ȵ���ϵ��֮�ȣ��ݴ˷������
��4����ͼ���ƽ��ʱY��ת����Ϊ$\frac{Y�ı仯��}{��ʼ��}��100%$��
��� �⣺��1����ͼ����Կ�������Ӧ��X��Y�����ʵ�����С��Z�����ʵ������࣬��X��YΪ��Ӧ�ZΪ������ҡ�n��X������n��Y������n��Z��=0.1mol��0.3mol��0.4mol=1��3��4����Ӧ�Ļ�ѧ����ʽΪ��X+3Y?4Z��
�ʴ�Ϊ��X+3Y?4Z��
��2��v��X��=$\frac{\frac{0.3}{5}}{2}$=0.03mol•��L•min��-1���ʴ�Ϊ��0.03mol•��L•min��-1��
��3��a��ÿ����3molX��ͬʱ����1molY�������ֵ�����Ӧ���ʴ���
b������������ȣ�������ѹǿʼ�ձ��ֲ��䣬�ʴ���
c��Z��Ũ�Ȳ��ٱ仯��˵�����淴Ӧ������ȣ�����ȷ��
d�������ڻ��������ܶ�ʼ�ձ��ֲ��䣬�ʴ���ѡ��c��
��4��ƽ��ʱY��ת����Ϊ$\frac{Y�ı仯��}{��ʼ��}��100%$=$\frac{1-0.9}{1}$��100%=10%���ʴ�Ϊ��10%��
���� ���⿼�黯ѧƽ��ͼ�������Ŀ����Ŀ�ѶȲ���ע����������ʵ����ı仯���ߣ����ջ�ѧ����ʽ���жϷ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
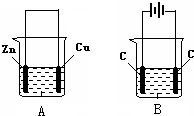 ����ͼ��ʾ�������ձ��зֱ�ʢ��������ϡ������Һ���Ȼ�ͭ��Һ��
����ͼ��ʾ�������ձ��зֱ�ʢ��������ϡ������Һ���Ȼ�ͭ��Һ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵĻ�ѧʽΪCO2 | |
| B�� | ������۷е�ߡ�Ӳ�ȴ� | |
| C�� | ������̼ԭ������C-O��ѧ����֮��Ϊ1��4 | |
| D�� | �����ʵ������������̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
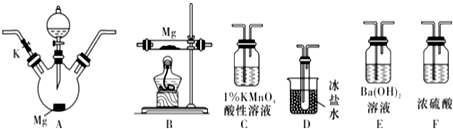
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ȶ��ԣ�HF��HCl | B�� | ������ǿ����K��Na | ||
| C�� | ����ǿ����H3PO4��H2SO4 | D�� | ����ǿ����NaOH��Mg��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH4HCO3������ķ�Ӧ�Ƿ��ȷ�Ӧ | |
| B�� | �÷�Ӧ�У�����ת��Ϊ�����ڲ������� | |
| C�� | ��Ӧ�������������������������� | |
| D�� | ÿ����0.1molNH4HCO3�ų�2.24L CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������¶Ȳ���������£��淴Ӧ����ѹǿ���½���һ��ʱ���ѹǿ���ֺ㶨���� | |
| B�� | m��n��w=3��1��2 | |
| C�� | ��λʱ���ڷ�Ӧ��Ũ�ȵļ��ٵ���������Ũ�ȵ����� | |
| D�� | ��������¶Ȳ���������£�����ǰ10 s��A������xmol������ͬ�����£�ǰ20 s����С��2x mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Һ�п��ܴ�������Fe3+��K+��Cl-��SO42- | |
| B�� | ��״���£���1.12LCO2����ͨ��1L0.1mol/l��NaAlO2��Һ�У�CO2+2H2O+AlO2-=Al��OH��3��+HCO3- | |
| C�� | ��ˮ�������c��H+��=1��10-12mol/L����Һ�п��ܴ�������K+��I-��Mg2+��NO3- | |
| D�� | ��NH4Al��SO4��2��Һ�еμ�Ba��OH��2��ҺʹSO42-��ȫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{c��{H}^{+}��}{c��C{H}_{3}COOH��}$ | B�� | $\frac{c��C{H}_{2}CO{O}^{-}��}{c��C{H}_{3}COOH��}$ | ||
| C�� | $\frac{c��O{H}^{-}��}{c��{H}^{+}��}$ | D�� | $\frac{c��{H}^{+}��•c��C{H}_{2}CO{O}^{-}��}{c��C{H}_{3}COOH��}$ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com