
ЁОЬтФПЁПСЊЕЊЃЈN2H4ЃЉгжГЦыТЃЌЫќгыN2O4ГЃгУзїЛ№М§ЭЦНјМСЁЃ
ЃЈ1ЃЉУРЙњМгРћИЃФсбЧДѓбЇЪЅЕибЧИчЕФGЁЄ NЁЄSChrauzerЕШШЫгУЕЊКЭЫЎеєЦјдкДЅУНЩЯЙтееЩфЯТКЯГЩИпФмЦјЬЌСЊЕЊГѕЛёГЩЙІЁЃЪдаДГіИУЗДгІЕФШШЛЏбЇЗНГЬЪНЃК_________ЁЃ
ЛЏбЇНЁ | МќФм/KJЁЄmol-1 |
N-H | 391 |
H-O | 463 |
O=O | 496 |
NЁдN | 946 |
N-N | 159 |
ЃЈ2ЃЉЫЎКЯСЊЕЊЃЈN2H4ЁЄH2OЃЉОпгаКмЧПЕФЛЙдадЁЃЙЄвЕЩЯгУЫЎКЯСЊАБЛЙдЗЈжЦШЁЕтЛЏФЦЙЬЬхЁЃЦфВйзїЪЧНЋЕЅжЪЕтМгШЫNaOHШмвКжаНјааЗДгІКѓдйМгШыЫЎКЯСЊЕЊЃЈвЊЩдЮЂЙ§СПЃЉНјааЗДгІЁЃвбжЊЃКN2H4ЁЄH2Oдк100Ёц вдЩЯЗжНтЁЃ
Ђй дкжЦБИNaIЕФЙ§ГЬжаЃЌПЩФмЛьгаЕФЮяжЪЪЧ_______ЃЌЩњВњЙ§ГЬжавЊЪЪЕБВЙГфNaOHЃЌФПЪЧ___________ЃЛ
Ђк ЮЊСЫЗРжЙЫЎКЯСЊАБИпЮТЗжНтЃЌЗДгІЮТЖШПижЦдк60-70ЁцЃЌЮТЖШвВВЛФмЙ§ЕЭЃЎЦфдвђЪЧ______ЃЛ
Ђл ЙЄвЕЩЯвВПЩвдгУСђЛЏФЦЛђЬњаМЛЙдЕтЫсФЦжЦБИЕтЛЏФЦЃЌЕЋЫЎКЯСЊАБЛЙдЗЈжЦЕУЕФВњЦЗДПЖШИќИпЃЌЦфдвђЪЧ___________
ЃЈ3ЃЉ325KЁЂЦ№ЪМбЙЧПЮЊ100kPaЪБЃЌдкКуШнЕФУмБеШнЦїжаГфШы4.6 g NO2,ЗЂЩњЗДгІЃК
2NO2(g) ![]() N2O4(g)ЃЌДяЕНЦНКтКѓШнЦїФкЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЮЊ57.5ЁЃ
N2O4(g)ЃЌДяЕНЦНКтКѓШнЦїФкЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЮЊ57.5ЁЃ
Ђй NO2гыN2O4ЕФЯћКФЫйТЪгыЦфХЈЖШЕФЙиЯЕШчЭМЫљЪОЃЌЭМжаНЛЕуAБэЪОИУЗДгІЫљДІЕФзДЬЌЮЊ________ЃЛ
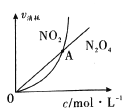
AЃЎЦНКтзДЬЌ BЃЎГЏе§ЗДгІЗНЯђвЦЖЏ CЃЎГЏФцЗДгІЗНЯђвЦЖЏ DЃЎЮоЗЈХаЖЯ
Ђк ЦНКтЪБNO2ЕФзЊЛЏТЪЮЊ_______ЃЌДЫЬѕМўЯТЕФKp=_______ЃЈKpгУЦНКтЗжбЙДњЬцЦНКтХЈЖШМЦЫуЃЌЗжбЙ=змбЙЁСЮяжЪЕФСПЗжЪ§ЃЉЁЃ
ЁОД№АИЁП N2(g)+2H2O(g)= N2H4(g)+O2(gЃЉЁїH=ЃЋ579 kJЁЄmol-1 NaIO3, ДйЪЙЗДгІЯђЩњГЩЮяЗНЯђНјаа ЮТЖШЙ§ЕЭЃЌЗДгІЫйТЪНЕЕЭ N2H4ЁЄH2OБЛбѕЛЏКѓЕФВњЮяЮЊN2КЭH2OЃЌВЛв§ШыдгжЪ B 40% 0.0056
ЁОНтЮіЁПЪдЬтЗжЮіЃК(lЃЉЕЊЦјКЭЫЎеєЦјдкДЅУНЩЯЙтееЩфЯТКЯГЩИпФмЦјЬЌСЊЕЊКЭбѕЦјЃЌИљОнЗДгІЮяЕФзмМќФм-ЩњГЩЮяЕФзмМќФм=ьЪБфЃЌаДИУЗДгІЕФШШЛЏбЇЗНГЬЪНЃЛ
(2ЃЉЫЎКЯСЊЕЊЃЈN2H4ЁЄH2OЃЉОпгаКмЧПЕФЛЙдадЁЃЙЄвЕЩЯгУЫЎКЯСЊАБЛЙдЗЈжЦШЁЕтЛЏФЦЙЬЬхЁЃЦфВйзїЪЧНЋЕЅжЪЕтМгШЫNaOHШмвКжаНјааЗДгІКѓдйМгШыЫЎКЯСЊЕЊЃЈвЊЩдЮЂЙ§СПЃЉНјааЗДгІЁЃвбжЊЃКN2H4ЁЄH2Oдк100Ёц вдЩЯЗжНтЁЃ
Ђй ЕтгыЧтбѕЛЏФЦЗДгІЩњГЩЕтЛЏФЦКЭЕтЫсФЦЃЌЩњВњЙ§ГЬжавЊЪЪЕБВЙГфNaOHЃЌПЩвдДйЪЙЗДгІе§ЯђНјааЃЛ
ЂкЮТЖШдНЕЭЃЌЗДгІЫйТЪдНТ§ЃЛ
ЂлЫЎКЯСЊАБЛЙдЕтЫсФЦбѕЛЏВњЮяЪЧЕЊЦјЃЛ
(3) 4.6 g NO2ЕФЮяжЪЕФСПЮЊ0.1molЃЌИљОнДяЕНЦНКтКѓШнЦїФкЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЮЊ57.5ЃЌПЩМЦЫуЦНКтКѓШнЦїжаЦјЬхзмЮяжЪЕФСП![]() ЃЌРћгУЁАШ§ЖЮЪНЁБдйЧѓГіЦНКтЪБNO2ЁЂ N2O4ЮяжЪЕФСПЁЃ
ЃЌРћгУЁАШ§ЖЮЪНЁБдйЧѓГіЦНКтЪБNO2ЁЂ N2O4ЮяжЪЕФСПЁЃ
НтЮіЃК(lЃЉЕЊЦјКЭЫЎеєЦјдкДЅУНЩЯЙтееЩфЯТКЯГЩИпФмЦјЬЌСЊЕЊКЭбѕЦјЃЌЛЏбЇЗНГЬЪНЮЊN2+2H2O= N2H4+O2ЃЌИљОнЗДгІЮяЕФзмМќФм-ЩњГЩЮяЕФзмМќФм=ьЪБфЃЌЁїH = 946+463ЁС4 - 391ЁС4 ЈC 159 -496 = ЃЋ579 kJЁЄmol-1 ЃЌЫљвдИУЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊN2(g)+2H2O(g)= N2H4(g)+O2(gЃЉЁїH=ЃЋ579 kJЁЄmol-1ЃЛ
(2ЃЉЂй ЕтгыЧтбѕЛЏФЦЗДгІЩњГЩЕтЛЏФЦКЭЕтЫсФЦЃЌЫљвддкжЦБИNaIЕФЙ§ГЬжаЃЌПЩФмЛьгаЕФЮяжЪЪЧNaIO3ЃЌЩњВњЙ§ГЬжавЊЪЪЕБВЙГфNaOHЃЌПЩвдДйЪЙЗДгІе§ЯђНјааЃЛ
ЂкЮТЖШдНЕЭЃЌЗДгІЫйТЪдНТ§ЃЌЫљвдЮТЖШВЛФмЙ§ЕЭЃЛ
ЂлЫЎКЯСЊАБЛЙдЕтЫсФЦбѕЛЏВњЮяЪЧЕЊЦјЃЌВЛв§ШыдгжЪЃЛ
(3) ЂйЭМжаНЛЕуAБэЪОЕФЯћКФЫйТЪvЃЈN2O4ЃЉ=vЃЈNO2ЃЉЃЌЖјДяЕНЦНКтЪБNO2ЕФЯћКФЫйТЪгІИУЪЧN2O4ЯћКФЫйТЪЕФ2БЖЃЌvЃЈNO2ЃЉ=2vЃЈN2O4ЃЉЃЌвђДЫДЫЪБvФцЃМvе§ЃЌЫљвдЗДгІЯђе§ЗДгІЗНЯђвЦЖЏЃЌЙЪбЁBЃЛ
4.6 g NO2ЕФЮяжЪЕФСПЮЊ0.1molЃЌИљОнДяЕНЦНКтКѓШнЦїФкЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЮЊ57.5ЃЌПЩМЦЫуЦНКтКѓШнЦїжаЦјЬхзмЮяжЪЕФСП![]() ЃЌ
ЃЌ
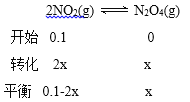
0.1-2x+ x=0.08 ЃЌx=0.02mol
Ђк ЦНКтЪБNO2ЕФзЊЛЏТЪЮЊ![]() ЃЌЦ№ЪМЮяжЪЕФСПЮЊ0.1molЃЌбЙЧПЮЊ100kPaЃЌЦНКтЪБЮяжЪЕФСПЮЊ0.08molЃЌбЙЧПЮЊ80kPaЃЌ, Kp=
ЃЌЦ№ЪМЮяжЪЕФСПЮЊ0.1molЃЌбЙЧПЮЊ100kPaЃЌЦНКтЪБЮяжЪЕФСПЮЊ0.08molЃЌбЙЧПЮЊ80kPaЃЌ, Kp=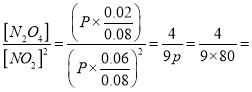 0.0056ЃЛ
0.0056ЃЛ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаИїзщЮяжЪЃЌАДЕЅжЪЁЂбѕЛЏЮяЕФЫГађХХСаЕФЪЧЃЈ ЃЉ
A. АБЦјЁЂЧтЦј B. ЩеМюЁЂбѕЛЏИЦ C. ЕЊЦјЁЂЕЈЗЏ D. вКТШЁЂЫЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈжае§ШЗЕФЪЧЃЈ ЃЉ
A. дкМвПЩгУЪГДзРДдіЧПЦЏАзЗлЕФЦЏАзад
B. вКЛЏЪЏгЭЦјЁЂЦћгЭЁЂЕиЙЕгЭМгЙЄжЦГЩЕФЩњЮяВёгЭЖМЪЧЬМЧтЛЏКЯЮя
C. ЮЊЮРаЧЙЉЕчЕФЬЋбєФмЗЋАхЃЈгыЬЋбєФмЕчГидРэЯрЫЦЃЉжївЊгЩЖўбѕЛЏЙшжЦГЩ
D. вНгУОЦОЋКЭЦЯЬбЬЧзЂЩфвКПЩгУЖЁДяЖћаЇгІЧјЗж
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌНЋЕШЬхЛ§ЕФбЮЫсКЭАБЫЎЗжБ№МгЫЎЯЁЪЭЃЌШмвКЕФЕМЕчадгыШмвКЬхЛ§ЕФБфЛЏЧњЯпШчЭМЫљЪОЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
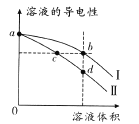
A. ЧњЯпЂђБэЪОАБЫЎМгЫЎЯЁЪЭЙ§ГЬжаШмвКЕМЕчадЕФБфЛЏ
B. ШмвКЕФpHДѓаЁЙиЯЕЃКc>b>d
C. гЩЫЎЕчРыГіЕФOH-: b>c
D. ШєНЋbЁЂdСНЕуШмвКЛьКЯЃЌдђЃКc(Cl-)>c(NH4+)>c(H+)>c(OH-)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПNa2OЁЂNaOHЁЂNa2CO3ЁЂNaClЁЂNa2SO4ПЩАДФГжжБъзМЛЎЗжЮЊЭЌвЛРрЮяжЪЃЌЯТСаЗжРрБъзМе§ШЗЕФЪЧ
ЂйФЦЕФЛЏКЯЮя ЂкФмгыЯѕЫсЗДгІЕФЮяжЪ ЂлЕчНтжЪ ЂмФЦбЮ ЂнФЦЕФКЌбѕЛЏКЯЮя
A. ЂйЂм B. ЂлЂм C. ЂкЂн D. ЂйЂл
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПбЮЫсЁЂЯѕЫсЁЂСђЫсдкЙЄвЕЩњВњжаОпгаживЊЕФзїгУЁЃ
ЃЈ1ЃЉЁАЭѕЫЎЁБЪЧХЈбЮЫсКЭХЈЧЭЫсАДЬхЛ§БШ3: lзщГЩЕФЛьКЯЮяЃЌЁАЭѕЫЎЁБШмН№ЕФдРэЮЊHNO3+3HCl=Cl2+NOCl+2H2OЃЌН№РызггыТШРызгаЮГЩAuCl4-РызгЃЌдіЧПСЫН№ЪєЕФЛЙдФмСІЁЃ
Ђй ЪдаДГіН№гыЭѕЫЎЗДгІЩњГЩH[AuCl4]ЕФЛЏбЇЗНГЬЪНЃК_________ЃЛЦфжаAuCl4-ЕФХфЮЛЪ§ЪЧ________;
Ђк вбжЊЃКNOClЕФШлЕу-645ЁцЃЌЗаЕу-5.5ЁцЃЌNOClЙЬЬхЕФОЇЬхРраЭЪЧ__________ЃЛ
Ђл зщГЩNOClЗжзгЕФШ§жждЊЫижаЃЌЕчИКадN_____OЃЈЬюЁА>ЁБЁЂЁА<ЁБЛђЁА=ЁБ)ЃЛШлЗаЕуH2O____NH3ЃЈЬюЁА>ЁБЁЂЁА<ЁБЛђЁА=ЁБ)ЃЛгыNH3ЛЅЮЊЕШЕчзгЬхЕФбєРызгга________ЃЈаДГівЛжжМДПЩЃЉЁЃ
ЃЈ2ЃЉЯѕЫсдкгаЛњЗДгІжавВгаживЊгУЭОЁЃTNTеЈвЉЁЂПрЮЖЫсЪЧЯѕЫсгыМзБНЁЂБНЗгЗЂЩњШЁДњЗДгІжЦГЩЕФЁЃЦфжаМзБНЗжзгжаЬМдзгЕФдгЛЏЗНЪНЮЊ______, 1molМзБНЗжзгжаКЌгаІвМќЕФЪ§ФПЮЊ_____ЃЛЪдНтЪЭдкЫЎжаБНЗгШмНтЖШДѓгкМзБНЕФдвђ________ЁЃ
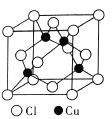
ЃЈ3ЃЉдкЯѕЫсЙЄвЕжагавЛжжживЊН№ЪєМДЮЊCuЃЌCuClОЇАћНсЙЙШчЭМЫљЪОЁЃвбжЊИУОЇЬхЕФУмЖШЮЊІбgЁЄcm-3ЃЌАЂЗќМгЕТТоГЃЪ§ЮЊNAЃЌдђИУОЇАћБпГЄЮЊ_______pm ЃЈжЛаДМЦЫуЪНЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙ§ГЬДцдкОЩЛЏбЇМќЖЯСбКЭаТЛЏбЇМќаЮГЩЕФЪЧ
A. ЫЎЕФЗжНт B. АБЦјвКЛЏ C. ИЩБљЩ§ЛЊ D. вКЕЊЦћЛЏ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЗМЯуЬўAЪЧвЛжжЛљБОЛЏЙЄдСЯЃЌПЩвдДгУККЭЪЏгЭжаЕУЕНЁЃOPAЪЧвЛжжживЊЕФгаЛњЛЏЙЄжаМфЬхЃЌAЁЂBЁЂCЁЂDЁЂEЁЂFКЭOPAЕФзЊЛЏЙиЯЕШчЯТЫљЪОЃК

вбжЊЃК![]()
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉAЕФЛЏбЇУћГЦЪЧ______ЁЃ
ЃЈ2ЃЉаДГіЩњГЩCЫљгаПЩФмЕФНсЙЙМђЪН________________________________ЁЃ
ЃЈ3ЃЉOPAОжаМфЬхEПЩКЯГЩвЛжжОлѕЅРрИпЗжзгЛЏКЯЮяFЃЌаДГіEЁњFЕФЗДгІЕФЛЏбЇЗНГЬЪН______________________________________ЃЌИУЗДгІЕФЗДгІРраЭЪЧ____________ЁЃ
ЃЈ4ЃЉгУЮФзжМђЪівјАБШмвКЕФХфжЦЗНЗЈЃКШЁlmL2%ЕФ__________ШмвКгкНрОЛЕФЪдЙмжаЃЌШЛКѓБпеёЕДБпж№ЕЮЕЮШы2%ЕФ ___________ЃЌжС____________________________ЮЊжЙЁЃ
аДГіOPAгызуН№вјАБШмвКЗДгІЕФРызгЗНГЬЪН_______________________________________ЁЃ
ЃЈ5ЃЉЗМЯуЛЏКЯЮяGЪЧEЕФЭЌЗжвьЙЙЬхЃЌGЗжзгжаКЌгаШЉЛљЁЂѕЅЛљКЭУбЛљШ§жжКЌбѕЙйФмЭХЃЌаДГіGШЮвтвЛжжПЩФмЕФНсЙЙМђЪН__________________ЁЃ
ЃЈ6ЃЉD(СкБНЖўМзЫсЖўввѕЅ)ЪЧвЛжждіЫмМСЁЃаДГігУAЁЂКЯЪЪЕФгаЛњЮяМАЮоЛњЪдМСЮЊдСЯЃЌОСНВНЗДгІКЯГЩDЕФТЗЯп_____________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПAЁЊFЪЧМИжжЕфаЭгаЛњДњБэЮяЕФЗжзгФЃаЭЃЌЧыПДЭМЛиД№ЯТСаЮЪЬтЁЃ
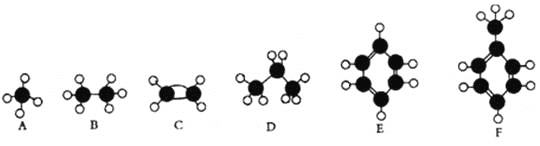
ЃЈ1ЃЉГЃЮТЯТКЌЬМСПзюИпЕФЦјЬЌЬўЪЧ________ЃЈЬюЖдгІзжФИЃЉЃЛ
ЃЈ2ЃЉФмЙЛЗЂЩњМгГЩЗДгІЕФЬўга ___________ЃЈЬюЪ§зжЃЉжжЃЛ
ЃЈ3ЃЉвЛТБДњЮяжжРрзюЖрЕФЪЧ ___________ЃЈЬюЖдгІзжФИЃЉЃЛ
ЃЈ4ЃЉаДГіЪЕбщЪвжЦШЁCЕФЛЏбЇЗНГЬЪН _____________________________________________________ЃЛ
ЃЈ5ЃЉаДГіEЗЂЩњфхДњЗДгІЕФЛЏбЇЗНГЬЪН__________________________________________________ЃЛ
ЃЈ6ЃЉАДЯЕЭГУќУћЗЈЬюаДЯТСагаЛњЮяЕФУћГЦЃК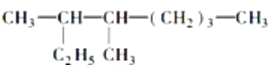 ЕФУћГЦЪЧЃК___________________________________________________________________ЁЃ
ЕФУћГЦЪЧЃК___________________________________________________________________ЁЃ
2ЃЌ6-ЖўМзЛљ-4-ввЛљ-2-аСЯЉЕФНсЙЙМђЪНЪЧЃК _____________________________________________ЃЌ
1molИУЬўЭъШЋШМЩеашЯћКФбѕЦј _______________ molЃЎ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com