
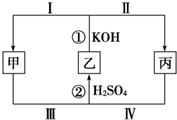
 ��ѧ����һ����ͬ��Ԫ��֮�䷢������ת�Ƶ�������ԭ��Ӧ�����ַ�Ӧ��ʱ������Һ����Եı仯���ı䷴Ӧ������ͼ��ʾ���ס��ҡ������������к���ͬһ��Ԫ�أ�
��ѧ����һ����ͬ��Ԫ��֮�䷢������ת�Ƶ�������ԭ��Ӧ�����ַ�Ӧ��ʱ������Һ����Եı仯���ı䷴Ӧ������ͼ��ʾ���ס��ҡ������������к���ͬһ��Ԫ�أ����� ��1��������ΪCl2����ΪKClO��Cl2��KOH��Ӧ����KCl��KClO��
����������Һ�У�KCl��KClO����������ԭ��Ӧ����Cl2��H2O���÷�Ӧ��ClԪ�ػ��ϼ���-1�ۡ�+1�۱�Ϊ0�ۣ�ʧ���ӵ�ClԪ�ر��������õ��ӵ�ClԪ�ر���ԭ��
��ԭ����У������ϵõ��ӷ�����ԭ��Ӧ��
��2�����ס��ҡ�����������ͬԪ��X�Ļ��ϼ۷ֱ�Ϊa��b��c����a��b��c����Ӧ�ٽ��й���������Ԫ�ػ��ϼ۲��䣬����ת�Ƶ�����ȼ�����������ͻ�ԭ������XԪ�ص����ʵ���֮�ȣ�
��� �⣺��1��������ΪCl2����ΪKClO��Cl2��KOH��Ӧ����KCl��KClO�����Լ�ΪKCl���ʴ�Ϊ��KCl��
����������Һ�У�KCl��KClO����������ԭ��Ӧ����Cl2��H2O���÷�Ӧ��ClԪ�ػ��ϼ���-1�ۡ�+1�۱�Ϊ0�ۣ�ʧ���ӵ�ClԪ�ر��������õ��ӵ�ClԪ�ر���ԭ����Ӧ����ʽΪKCl+KClO+H2SO4=K2SO4+Cl2��+H2O��KCl��ClԪ�ر�������KClO��ClԪ�ر���ԭ�����Ա������ͱ���ԭ��Cl������֮�ȵ����������֮��Ϊ1��1��
�ʴ�Ϊ��KCl+KClO+H2SO4=K2SO4+Cl2��+H2O��1��1��
��ԭ����У������ϵõ��ӷ�����ԭ��Ӧ������KClʱ�õ��ӷ�����ԭ��Ӧ������������Ӧ����ΪI��
�ʴ�Ϊ��I��
��2�����ס��ҡ�����������ͬԪ��X�Ļ��ϼ۷ֱ�Ϊa��b��c����a��b��c����Ӧ�ٽ��й���������Ԫ�ػ��ϼ۲��䣬ÿ��X�õ�����Ϊ��b-a����ÿ��Xʧ������Ϊ��c-b��������ת�Ƶ�����ȵã�ʧ���Ӻ͵õ��ӵ�X֮��Ϊ��b-a������c-b������������ͻ�ԭ������X�����ʵ���֮�ȵ��ڻ�ԭ���������������ʵ���֮��Ϊ��b-a������c-b�����ʴ�Ϊ����b-a������c-b����
���� ���⿼�������ƶϣ�Ϊ��Ƶ���㣬���ؿ������ԭ�����漰������ԭ��Ӧ��ԭ���ԭ������ȷ������ԭ��Ӧ��ת�Ƶ�������ǽⱾ��ؼ����ѵ��ǣ�2������㣬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.022mol•L-1 | B�� | 0.045 mol•L-1 | C�� | 0.8 mol•L-1 | D�� | 0.1 mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��FeCl2��Һ��ͨ��Cl2��Fe2++Cl2=Fe3++2Cl- | |
| B�� | Fe��OH��2����ϡHNO3�У�Fe��OH��2+2H+=Fe2++2H2O | |
| C�� | Fe2O3���������������Fe2O3+6H++2Br-�T2Fe2++Br2+3H2O | |
| D�� | HCl����NaAlO2��Һ�У�AlO2-+H++H2O=Al��OH��3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 5.6 g��������������ȫ��Ӧת�Ƶĵ�����Ϊ0.2NA | |
| B�� | 100 mL 2.0 mol•L-1�������������Һ�������Ӿ�Ϊ0.2NA | |
| C�� | ��״���£�22.4 L CO2��22.4 L H2O����ԭ������Ϊ3 NA | |
| D�� | ����ֱ�Ϊ1.0L pH=2��������������Һ������������Ϊ0.01NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ñ���ʳ��ˮ��Ũ���Ṳ���Ʊ�HCl���� | |
| B�� | ��H2��Cl2��ϣ��ڹ��������·�Ӧ�����ڹ�ҵ�Ʊ����� | |
| C�� | ��Cl2ͨ�뱥��ʯ��ˮ�����ڹ�ҵ����Ư�� | |
| D�� | ʵ������ϡNaOH��Һ����ʵ������ж����Cl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
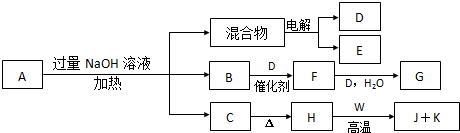
 ����0.1mol��MnO2��ĩ��50mL�����������Һ�У��ڱ�״���·ų�����������ʱ��Ĺ�ϵ��ͼ��ʾ��5���ӷ�Ӧ��ɣ����ش��������⣺
����0.1mol��MnO2��ĩ��50mL�����������Һ�У��ڱ�״���·ų�����������ʱ��Ĺ�ϵ��ͼ��ʾ��5���ӷ�Ӧ��ɣ����ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com