
| 阶段 | 相当于电解什么溶液 | 离子方程式 |
| ① | | |
| ② | | |
| ③ | | |
| ④ | | |
| ⑤ | | |
科目:高中化学 来源:不详 题型:单选题
| A.电解熔融的氧化铝制取金属铝,用铁作阳极 | B.电解法精炼粗铜,用纯铜作阴极 |
| C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 | D.在镀件上电镀锌,用锌作阳极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题: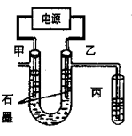
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.a 为电源的正极 |
| B.通电一段时间后,石墨电极附近溶液先变红 |
| C.Fe电极的电极反应是4OH-- 4e-=2H2O+O2↑ |
D.电解饱和食盐水的总反应是: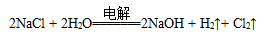 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
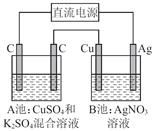
| A.0.05 mol/L | B.0.035 mol/L | C.0.025 mol/L | D.0.020 mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
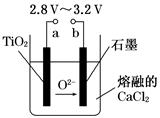
| A.a为电源的正极 |
| B.石墨电极上发生还原反应 |
| C.阴极发生的反应为:TiO2+4e-=Ti+2O2- |
| D.每生成0.1 mol钛,转移电子0.2 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.a为直流电源的负极 |
| B.阴极的电极反应式为:2HSO3-+2H++e-=S2O42-+2H2O |
| C.阳极的电极反应式为:SO2+2H2O-2e-=SO42-+4H+ |
| D.电解时,H+由阴极室通过阳离子交换膜到阳极室 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com