
| A、分别充满HCl、NH3的烧瓶倒置于水中后液面迅速上升,说明二者均易溶于水 | ||||||
B、向NH4HCO3溶液中加过量的NaOH溶液并加热,离子方程式为:NH
| ||||||
| C、用NH4Cl固体和Ca(OH)2固体制备并收集NH3,需要的玻璃仪器有酒精灯、大试管、导管、集气瓶 | ||||||
| D、用湿润的红色石蕊试纸检验氨气 |


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
A、CH4+Cl2
| |||
| B、2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ | |||
C、
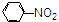 | |||
D、nCH2=CH2
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HA能与水以任意比互溶 |
| B、0.1mol?L-1HA溶液的pH约为3 |
| C、HA可与NaHCO3反应放出CO2 |
| D、HA溶液的导电能力很差 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol?L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com