
| A. | Al(OH)3 | B. | Al2O3 | C. | SiO2 | D. | Al |
科目:高中化学 来源: 题型:选择题
| A. | 反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 | |
| B. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| C. | CH3COOH 溶液加水稀释后,溶液中C(OH-)减小 | |
| D. | Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH 减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2晶体和SiO2晶体中,微粒之间的化学键类型相同,晶体类型也相同 | |
| B. | H2S分子中,所有原子的最外层都达到了8电子的稳定结构 | |
| C. | 碘单质升华过程中不存在化学键被破坏的过程 | |
| D. | NaCl气体溶于水后,因为共价键被破坏,从而形成了Na+和Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
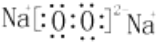
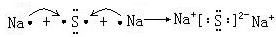
 、其最高价氧化物对应的水化物的化学式H3PO4.
、其最高价氧化物对应的水化物的化学式H3PO4.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何化学反应都伴随着能量的变化 | |
| B. | H2O(气)-→H2O(液)该过程放出大量的热,所以该过程是化学变化 | |
| C. | 化学反应中能量的变化都表现为热量的变化 | |
| D. | 所有的物质一定存在化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时正极附近溶液的碱性减弱 | |
| B. | 放电时,电子由Zn经导线转移到K2FeO4 | |
| C. | 放电时每转移3mol电子,正极有1mol K2FeO4被还原 | |
| D. | 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com