
分析 (1)原子基态时最外层具有6个p电子,s能级容纳2个电子,则最外层电子数为8;
(2)原子基态时n=4的电子层有2个电子,3d轨道上有5个电子,基态原子外围电子排布为3d54s2;
(3)原子基态时次外层d轨道全满,最外层有一个s电子,基态原子外围电子排布为nd10ns1;
(4)某元素+3价离子基态时和氩原子的电子构型相同,该元素质子数=18+3=21;
(5)某元素+3价离子基态时的3d轨道半充满,则基态原子外围电子排布为3d64s2.
解答 解:(1)原子基态时最外层具有6个p电子,s能级容纳2个电子,则最外层电子数为8,处于零族,故答案为:具有p6(即np6)排布的是稀有气体元素(He除外);
(2)原子基态时n=4的电子层有2个电子,3d轨道上有5个电子,基态原子外围电子排布为3d54s2,为Mn元素,故答案为:Mn;
(3)原子基态时次外层d轨道全满,最外层有一个s电子,基态原子外围电子排布为nd10ns1,处于ⅠB族,
故答案为:ⅠB族;
(4)某元素+3价离子基态时和氩原子的电子构型相同,该元素质子数=18+3=21,为Sc元素,
故答案为:Sc;
(5)某元素+3价离子基态时的3d轨道半充满,则基态原子外围电子排布为3d64s2,为Fe元素,
故答案为:Fe.
点评 本题考查核外电子排布以及结构与性质、位置关系,难度不大,注意对核外电子排布规律的理解掌握.


科目:高中化学 来源: 题型:实验题
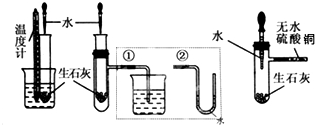
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若向2mL 1mol/LNaOH溶液中先加入2滴1mol/L MgCl2溶液,再加入2滴1mol/L的FeCl3溶液,可以证明Mg(OH)2沉淀转化为Fe(OH)3沉淀 | |
| B. | 常温下,某溶液中由水电离出来的c(OH-)=1.0×10-12mol•L-1,则该溶液可能为盐酸,也可能为NaOH溶液 | |
| C. | 处理锅炉水垢中的CaSO4时,依次加入饱和NaCO3溶液和盐酸,水垢溶解,说明溶解度:S(CaCO3)<S(CaSO4) | |
| D. | 常温下的醋酸铵溶液呈中性,则溶液中c(H+)=c(OH-)=1.0×10-7mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转 | |
| B. | 能量低的电子只能在s轨道上运动,能量高的电子总是在f轨道上运动 | |
| C. | 能层序数越大,s原子轨道的半径越大 | |
| D. | 在同一能级上运动的电子,其运动状态可能相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 降低温度可以缩短反应达到平衡的时间 | |
| B. | 恒容时通入氩气,压强增大,平衡向右移动 | |
| C. | 恒容时通入X2,平衡向正反应方向移动,平衡常数不变 | |
| D. | 恒温恒压下,若混合气体密度不变,说明反应已达平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2+Na2SO4=BaSO4↓+2NaCl | B. | H2SO4+BaCl2═BaSO4↓+2HCl | ||
| C. | Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 | D. | BaCO3+H2SO4=BaSO4↓+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 互为同系物的有机物其组成元素相同,且结构必须相似 | |
| B. | 正戊烷分子中所有碳原子均在一条直线上 | |
| C. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| D. | 互为同系物的有机物其相对分子质量数值一定相差14 n(n为正整数) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com