
将1mol纯净的氨基甲酸铵(NH2COONH4)置于特制的真空密闭容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其分解达到平衡:NH2COONH4  2NH3(g)+CO2(g)(s-固态,g-气态)下列可以判断该反应己经达到化学平衡状态的是
2NH3(g)+CO2(g)(s-固态,g-气态)下列可以判断该反应己经达到化学平衡状态的是
A. 反应速率:v(正)=v(逆)=0 B. 有2molNH3生成
C. 气体的总体积保持不变 D. CO2的质量保持不变
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源:2017届浙江省高三“超级全能生”3月联考(选考科目)化学试卷(解析版) 题型:选择题
下列有关说法不正确的是
A. HC1溶于水后生成水合氢离子和水合氯离子
B. 焰色反应可以检测溶液中的钠离子、钾离子等,属于物理实验
C. 金属镁能在氮气、氧气、二氧化碳中燃烧
D. SO2能漂白品红溶液、红色石蕊试液、紫色高锰酸钾溶液等
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省六安市高一下学期第一次阶段检测化学试卷(解析版) 题型:推断题
现有A、B、C、D、E、F、G、H八种气体均为无机物,根据下列事实判断各是哪种气体。
①A、B、D、F四种气体是单质。
②把A和B混合,在光照下发生爆炸,生成气体C。
③A和D在一定条件下发生反应生成气体E。
④D和F在放电条件下可生成气体G。
⑤G与空气混合时,由无色变成红棕色气体H。
⑥E和C反应冒白烟。
⑦H溶于水生成一种强酸和气体G。
试写出各种气体的化学式:
A________,B_______,C________,D_______,E______,F_____,G_______,H_______。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一下学期期中考试化学试卷(解析版) 题型:填空题
任何一个化学反应中都会伴随能量变化和物质变化。
(1)下图为氢气和氧气生成1mol水蒸气时的能量变化情况。

生成1mol水蒸气时,形成新化学键所释放的总能量_____断开旧化学键所吸收的总能量(填“大于”“小于”或“等于”),因此水的分解反应为________(填“吸热”或“放热”)反应。
(2)随着科学技术的发展和社会进步,各种各样的电器不断进入现代社会,化学电源大大丰富和方便了我们的生活、学习和工作。原电池中发生的化学反应属于______。镁铝原电池,电解质用稀硫酸,则其负极的电极反应式为______;电解质用氢氧化钠溶液,电池工作时,溶液中的OH-移向_____极(“镁”或“铝”)。
(3)在三个容器均为2L的密闭容器中发生反应:2HI(g)  H2(g)+I2(g),已知H2(g)和I2(g)的起始物质的量均为0,HI(g)的物质的量(mol)随反应时间(min)的变化情况如下表所示,表中温度的单位为摄氏度(℃)。
H2(g)+I2(g),已知H2(g)和I2(g)的起始物质的量均为0,HI(g)的物质的量(mol)随反应时间(min)的变化情况如下表所示,表中温度的单位为摄氏度(℃)。
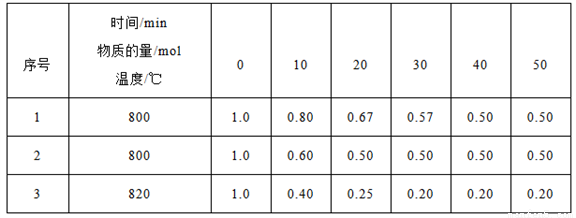
①实验1和实验2中,有一个实验使用了催化剂,则使用了催化剂的是实验_____(填“1”或“2”)。
②实验1中,20min~30min间生成I2(g)的平均反应速率为_____,实验3的反应达到化学反应限度时H2(g)物质的量的百分数为_______。
③下列物理量不再变化时,能判断实验3中反应达到化学反应限度的是__________。
A.混合气体颜色 B.混合气体密度 C.混合气体总压强
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一下学期期中考试化学试卷(解析版) 题型:选择题
对于可逆反应A(g)+3B(s) 2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
A.v(A)=0.5 mol·L-1·min-1 B.v(B)=1.2 mol·L-1·s-1
C.v(D)=0.4 mol·L-1·min-1 D.v(C)=0.1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一下学期期中考试化学试卷(解析版) 题型:选择题
当其他条件不变时,下列说法正确的是
A. 用粉术状锌代替块状锌与稀硫酸反应一定会加快反应速率
B. 使用催化剂一定能加快反应速率
C. 在合成氨反应中,增大N2浓度一定可以使H2全部转化为NH3
D. 当反应物与生成物浓度相等时,可逆反应一定己达到化学反应限度
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(一)化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A. 用FeCl3溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+
B. 向氨水中通入过量SO2:SO2+2NH3·H2O=2NH4++SO32-+H2O
C. 用MnO2与浓盐酸反应制Cl2:MnO2+4HCl Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
D. 在强碱性溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3+4OH-=2FeO43-+3Cl-+5H2O
查看答案和解析>>
科目:高中化学 来源:四川省成都市北湖校区2016-2017学年高一3月月考化学试卷 题型:填空题
填空题
(1)H、D、T三种原子,它们之间的关系是_________;在标准状况下,它们的单质的密度之比为_____;1 mol各单质中,它们的质子数之比为________;在标准状况下,1L各种单质中,它们的电子数之比为________。
(2)第116号元素(元素符号Lv)被中国科学技术名词审定委员会命名为垃,该元素在元素周期表中的位置是_____,属于______元素(填“金属”或“非金属”),若该元素存在最高价氧化物对应的水化物,则其化学式为_______。
(3)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。请把与下面元素有关性质相符的曲线标号(A~G)填入相应的空格中:
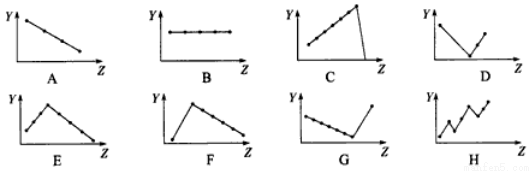
①IIA族元素的价电子数__________;②第三周期元素的最高正化合价____________;
③VIIA族元素氢化物的沸点____________。
(4)核内中子数为N的R2+,质量数为A,则ng它的相同价态氧化物中所含的电子的物质的量约为_____mol。
①若R为钙元素,且N=19,则采用原子符号的表达方式,可将R2+表示为_______;
②若R为第五周期IIA元素,则其硫酸盐______于水(填“溶”或“不溶”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com