
请回答下列问题:
(1)下列现象和应用与电子跃迁无关的是________________________________。
A.激光 B.焰色反应 C.原子光谱 D.燃烧放热 E.石墨导电
(2)A、B两种短周期元素,A是原子半径最小的元素,B原子最外层电子数是次外层的两倍。某平面正六边形分子由A、B两种元素组成且原子个数比为1:1,该分子中含有_______个σ键。
(3)元素铬化合物(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
①与铬同周期的基态原子中最外层电子数与铬原子相同的元素有___________(填元素符号)
②在a:苯 b:CH3OH c:HCHO d:CS2 e:CCl4 五种有机溶剂中,碳原子采取sp3杂化的分子有___________(填字母),CS2分子的键角是__________。
③过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O) 6]2+显粉红色。据此判断,[Mn(H2O) 6]]2+ _____________(填“无”或“有”)颜色
(4) 请写出HClO的电子式:_______________________;在下图配合物离子[Cu(NH3)4]2+.中的画出配位键:

(5) A、B均为短周期金属元素。依据下表数据和已学知识,
|
电离能/KJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
|
A |
932 |
1821 |
15390 |
21771 |
|
B |
738 |
1451 |
7733 |
10540 |
判断金属B的价电子电子排布式______,写出金属B与二氧化碳反应的化学方程式: _______________________________________________。
(1)D 、 E (2分,漏选得1分,有错选不得分)
(2) 12 (1分)
(3) ① Cu K (2分,写对一个给1分,全部写对得满分)
② b e (2分,漏选得1分,有错选不得分) 1800 (1分)
③ 有 (1分)
(4) 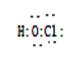
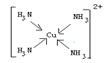 (各1分)、
(各1分)、
(5) 3s2(1分) 2Mg+CO2 ="==" 2MgO+C (2分)
【解析】
试题分析:(1)燃烧放热、石墨导电都与电子跃迁无关,故本题的答案选择DE;(2)A、B两种短周期元素,A是原子半径最小的元素,故A为H元素;B原子最外层电子数是次外层的两倍,所以B为C;某平面正六边形分子由A、B两种元素组成且原子个数比为1:1,该分子苯,所以其中含有12个σ键;(3)①与铬同周期的基态原子中最外层电子数与铬原子相同的元素有Cu 、K;②在a:苯 b:CH3OH c:HCHO d:CS2
e:CCl4 五种有机溶剂中,碳原子采取sp3杂化的分子b和e,而a和c中碳原子是采用sp2杂化,d中碳原子采用的是sp杂化,其分子结构为直线型,故CS2分子的键角是1800;③过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O) 6]2+显粉红色,其中Co为d7,[Mn(H2O) 6]]2+中Mn为d5,所以其有颜色;(4) 请写出HClO的电子式为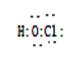 ;配合物离子[Cu(NH3)4]2+.中的配位键如下:
;配合物离子[Cu(NH3)4]2+.中的配位键如下: 注意的是铜离子提供空轨道,而氨气中的N原子提供孤独电子;(5) 从表可以推断出A、B分别为Na、Mg,所以B的价电子电子排布式为:3s2,镁与二氧化碳的反应的方程式为:2Mg+CO2
="==" 2MgO+C。
注意的是铜离子提供空轨道,而氨气中的N原子提供孤独电子;(5) 从表可以推断出A、B分别为Na、Mg,所以B的价电子电子排布式为:3s2,镁与二氧化碳的反应的方程式为:2Mg+CO2
="==" 2MgO+C。
考点:电子跃迁、杂化类型、电子式、配位键、电离能
点评:本题考查了电子跃迁、杂化类型、电子式、配位键、电离能,该题综合性强,难度中等。


科目:高中化学 来源: 题型:
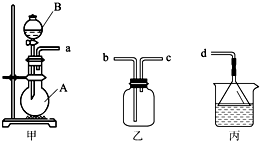 液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液.请回答下列问题:
液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 750-970oC | 通电,Na3AIF6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ((Ⅰ)某兴趣小组的同学用下图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:
((Ⅰ)某兴趣小组的同学用下图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流计的指针发生了偏转.请回答下列问题:
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com