
)磷酸燃料电池是目前较为成熟的燃料电池,其基本组成和反应原理如下。
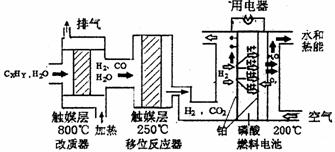
(1)在改质器中主要发生的反应为_______________________________
(2)移位反应器中CO(g)+H2O (g) 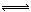 CO2 (g)+H2(g) ,在一定温度下,在1L容器中发生上述反应,各物质的物质的量浓度变化如下表:
CO2 (g)+H2(g) ,在一定温度下,在1L容器中发生上述反应,各物质的物质的量浓度变化如下表:
| t/min | COmol/L) | H2O(mol/L) | CO2(mol/L) | H2(mol/L) |
| 0 | 0.2 | 0.3 | 0 | 0 |
| 2 | n1 | n2 | n3 | 0.1 |
| 3 | n1 | n2 | n3 | 0.1 |
| 4 | 0.09 | 0.19 | 0.11 | 0.11 |
①此温度下,该反应的平衡常数为________
②反应在3~4 min之间,氢气的物质的量增多的原因可能是 (填代号)
A.充入水蒸汽 B.升高温度 C.使用催化剂 D.充入氢气
(3)磷酸燃料电池负极排出的气体主要是___ __,
该电池正极的电极反应为_ _ __。
(4)磷酸燃料电池的电极上镀了铂粉,这样做的目的,除了起到更好的导电作用外,还具备的作用是 。
(5)总体看来,整个体系中能量来自与CxHy与空气的反应,假设CxHy为辛烷,且
已知辛烷的燃烧热为5 518 kJ·mol-1,请写出辛烷燃烧热的热化学方程式 。
【知识点】燃料电池原理 化学平衡的移动 热化学方程式 F1 F3 G2
【答案解析】(1)CxHy+XH2O  XCO+(X+Y/2)H2
XCO+(X+Y/2)H2
(2)① 0.5② B
(3) CO2 O2 +4H++4e--=2H2O
(4) 增大电极单位面积吸附H2、O2分子数,加快反应速率
(5) C8H18(l)+ O2(g)===8CO2(g)+9H2O(l);ΔH=-5 518 kJ·mol-1
O2(g)===8CO2(g)+9H2O(l);ΔH=-5 518 kJ·mol-1
解析:(1)改质器中进入的物质是烃和水,反应温度是800℃,出来的气体是水、氢气和一氧化碳,所以发生的化学反应:CxHy+XH2O  XCO+(X+Y/2)H2(2)①根据氢气浓度增加了0.1mol/L, n1、n2、n3分别为0.1mol/L、0.2mol/L、0.1mol/L,k=
XCO+(X+Y/2)H2(2)①根据氢气浓度增加了0.1mol/L, n1、n2、n3分别为0.1mol/L、0.2mol/L、0.1mol/L,k= ;② 反应物的浓度都减小了0.1mol/L,生成物的浓度都增大了0.1mol/L,排除ADC,选B;(3)燃料电池中,负极上燃料失去电子发生氧化反应,二氧化碳是废气,所以排出的气体是二氧化碳,正极上氧化剂得电子和氢离子反应生成水,电极反应式为O2+4H++4e-=2H2O(4)磷酸燃料电池的电极上镀了铂粉,这样做的目的,除了起到更好的导电作用外,还具备的作用是增大电极单位面积吸附H2、O2分子数,加快反应速率,(5)根据燃烧热的定义及热化学方程式的要求得: C8H18(l)+
;② 反应物的浓度都减小了0.1mol/L,生成物的浓度都增大了0.1mol/L,排除ADC,选B;(3)燃料电池中,负极上燃料失去电子发生氧化反应,二氧化碳是废气,所以排出的气体是二氧化碳,正极上氧化剂得电子和氢离子反应生成水,电极反应式为O2+4H++4e-=2H2O(4)磷酸燃料电池的电极上镀了铂粉,这样做的目的,除了起到更好的导电作用外,还具备的作用是增大电极单位面积吸附H2、O2分子数,加快反应速率,(5)根据燃烧热的定义及热化学方程式的要求得: C8H18(l)+ O2(g)===8CO2(g)+9H2O(l);ΔH=-5 518 kJ·mol-1注意辛烷为液态,放热反应的ΔH为负。
O2(g)===8CO2(g)+9H2O(l);ΔH=-5 518 kJ·mol-1注意辛烷为液态,放热反应的ΔH为负。
【思路点拨】本题考查了燃料电池的基本原理,难度不大,注意电极反应式的书写要结合电解质溶液的酸碱性,电解质溶液的酸碱性不同,电极反应式可能不同。注意辛烷为液态,放热反应的ΔH为负。


科目:高中化学 来源: 题型:
已知“凡气体分子总数增多的反应一定是熵增大的反应”.根据所学知识判断,下列反应中,在所有温度下都不自发进行的( )
|
| A. | 2O3(g)═3O2(g)△H<0 | B. | 2CO(g)═2C(s)+O2(g)△H>0 |
|
| C. | N2(g)+3H2(g)═2NH3(g)△H<0 | D. | CaCO3(s)═CaO(s)+CO2(g)△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于卤素的叙述正确的是 ( )
A、随核电荷数增加卤素原子非金属性增强
B、随核电荷数增加,单质熔沸点升高
C、随核电荷数增加,单质氧化性增强
D、单质与水反应,均可用通式X2+H2O=HX+HXO表示
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,对于pH均为5的HCl溶液和NH4Cl溶液,下列说法正确的是 ( )。
A.两溶液稀释10倍后,pH相等
B.两溶液加热至相同的温度后,pH相等
C.两溶液中各加入等体积的pH等于9的NaOH溶液后,pH相等
D.两溶液中水的离子积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是一种可再生燃料。在容积为2L的密闭容器中进行反应:CO(g)+2H2(g)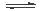 CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示。
CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示。
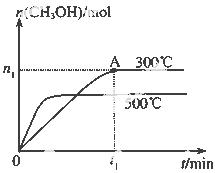
(1)该反应的△H 0 (填>、<或=)
(2)300℃时,0-t1 min内 CH3OH的平均生成速率为
(3)若要提高甲醇的产率,可采取的措施有_________ 。(填字母)
A.缩小容器体积 B.降低温度
C.升高温度 D.使用合适的催化剂
E.甲醇从混合体系中分离出来
(4)300℃时,CO、H2的起始物质的量分别为2mol和3mol,若图中n1数据为0.5mol,试计算300℃下,该反应的平衡常数(写出计算过程,保留两位有效数字)
(5)工业上也可以用CO2和H2反应制得甲醇。在2×105Pa、300℃的条件下,若有440g CO2与H2恰好完全反应生成甲醇和水,放出495kJ的热量,试写出该反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,反应N2(g)+O2(g)==2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是
A.降低体系温度 B.恒容,充入N2
C.恒容,充入He D.恒压,充入He
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下在容积为 2L 的密闭容器中,发生反应 2X(g) + Y(g)  2W(g);△H<0,当充入 2 mol X 和 1 mol Y,经20 s达到平衡时生成了 0.4 molW。下列说法正确的是()
2W(g);△H<0,当充入 2 mol X 和 1 mol Y,经20 s达到平衡时生成了 0.4 molW。下列说法正确的是()
①升高温度,W 的体积分数减小,△H 增大
②以 Y 的浓度变化表示的反应速率为 0.01 mol/(L·s)
③在其它条件不变的情况下,增加 1 mol X ,则 X 和 Y 的转化率均提高
④增大压强,正反应速率增大,逆反应速率减小,则平衡向正反应方向移动
⑤再向容器中通入 2 mol X 和 1 mol Y,达到平衡时,X、Y 的转化率均增大。
A、①⑤ B、⑤ C、②③④ D、④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
在某温度下,可逆反应mA+nB⇌pC+qD平衡常数为K,下列说法正确的是( )
|
| A. | K越大,达到平衡时,反应进行的程度越大 |
|
| B. | K越小,达到平衡时,反应物的转化率越大 |
|
| C. | K随反应物浓度的改变而改变 |
|
| D. | K随着温度的升高而增小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com