
| A、C2H6 |
| B、HCl |
| C、NH4Cl |
| D、Na2O2 |


科目:高中化学 来源: 题型:
| A、理论上任何放热的反应均能设计成为原电池 |
| B、实验室研究反应条件对速率的影响,硫代硫酸钠稀溶液与稀硫酸反应Na2S2O3+H2SO4=S↓+SO2↑+Na2SO4+H2O,常根据产生气泡的快慢判断反应速率的快慢 |
| C、恒温恒容,2molSO2(g)与1molO2(g)充分反应放出热量是aKJ,则该反应的热方程式是2SO2(g)+O2(g)?2SO3(g)△H=-akJ/mol |
| D、对于有气体参加的某放热反应,使用合适催化剂或增大压强(减小体积)均增加了单位体积内活化分子数目从而加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、11.2 g |
| B、25.2 g |
| C、16.8 g |
| D、33.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
| B、碳酸氢钠溶液与过量澄清石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| C、硫酸亚铁溶液中加入酸化的双氧水:Fe2++2H++H2O2=Fe3++2H2O |
| D、向明矾溶液中滴加过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
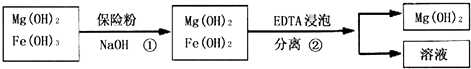
| 精制阻燃剂的条件 | 阻燃剂铁含量 | |||
| 序号 | 提纯体系温度/℃ | 加入EDTA质量/g | 加入保险粉质量/g | W(Fe)/(10-4g) |
| 1 | 40 | 0.05 | 0.05 | 7.63 |
| 2 | 40 | 0.05 | 0.10 | 6.83 |
| 3 | 60 | 0.05 | 0.10 | 6.83 |
| 4 | 60 | 0.10 | 0.10 | 6.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,
用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,| 实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
| 1 | 25.00 | 24.41 |
| 2 | 25.00 | 24.39 |
| 3 | 25.00 | 22.60 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com