
在101kPa时, 完全燃烧生成
完全燃烧生成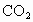 和液态
和液态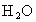 ,放出890kJ的热量,
,放出890kJ的热量,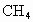 的燃烧热为多少?
的燃烧热为多少?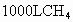 (标准状况)燃烧后所产生的热量为多少?
(标准状况)燃烧后所产生的热量为多少?
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
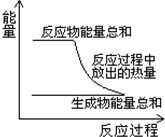 已知在101KPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-820KJ?mol-1.则下列说法中正确的是( )
已知在101KPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-820KJ?mol-1.则下列说法中正确的是( )| A、反应过程中的能量变化关系可如图所示 | B、11.2LCH4完全燃烧放出热量410KJ | C、CH4的燃烧热为820KJ | D、凡是有水生成的氧化还原反应都是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:022
在101kPa时,完全燃烧1g甲烷气体,生成液态水和二氧化碳气体能放出55.6kJ的热量,计算甲烷的燃烧热并写出甲烷燃烧的热化学方程式。如果燃烧5mol甲烷气体,能放出多少热量?
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com