
 Ӣ
Ӣ Ӣ
Ӣ Ӣ
Ӣ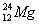 Ӣ
Ӣ Ӣ
”¢ ÖŠ£ŗ
ÖŠ£ŗ
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 ĖÄÖÜĘŚµÄŌŖĖŲ£¬ĖüĆĒµÄŗĖµēŗÉŹżA£¼B£¼C£¼D£¼E”£ĘäÖŠA”¢B
ĖÄÖÜĘŚµÄŌŖĖŲ£¬ĖüĆĒµÄŗĖµēŗÉŹżA£¼B£¼C£¼D£¼E”£ĘäÖŠA”¢B ”¢CŹĒĶ¬Ņ»ÖÜĘŚµÄ·Ē½šŹōŌŖĖŲ”£»ÆŗĻĪļDCŠĪ³ÉµÄ¾§ĢåĪŖĄė×Ó¾§Ģ壬DµÄ¶ž¼ŪŃōĄė×ÓÓėCµÄŅõĄė×Ó¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹”£AC2ĪŖ·Ē¼«ŠŌ·Ö×Ó”£B”¢CµÄĒā»ÆĪļµÄ·Šµć±ČĖüĆĒĶ¬×åĻąĮŚÖÜĘŚŌŖĖŲĒā»ÆĪļµÄ·Šµćøß”£EµÄŌ×ÓŠņŹżĪŖ29”£Ēėøł¾ŻŅŌÉĻĒéæö£¬»Ų“šĻĀĮŠĪŹĢā£ŗ£Ø“šĢāŹ±£¬A”¢B”¢C”¢D”¢EÓĆĖł
”¢CŹĒĶ¬Ņ»ÖÜĘŚµÄ·Ē½šŹōŌŖĖŲ”£»ÆŗĻĪļDCŠĪ³ÉµÄ¾§ĢåĪŖĄė×Ó¾§Ģ壬DµÄ¶ž¼ŪŃōĄė×ÓÓėCµÄŅõĄė×Ó¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹”£AC2ĪŖ·Ē¼«ŠŌ·Ö×Ó”£B”¢CµÄĒā»ÆĪļµÄ·Šµć±ČĖüĆĒĶ¬×åĻąĮŚÖÜĘŚŌŖĖŲĒā»ÆĪļµÄ·Šµćøß”£EµÄŌ×ÓŠņŹżĪŖ29”£Ēėøł¾ŻŅŌÉĻĒéæö£¬»Ų“šĻĀĮŠĪŹĢā£ŗ£Ø“šĢāŹ±£¬A”¢B”¢C”¢D”¢EÓĆĖł ¶ŌÓ¦µÄŌŖĖŲ·ūŗűķŹ¾£©
¶ŌÓ¦µÄŌŖĖŲ·ūŗűķŹ¾£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| A£®O4·Ö×ÓÄŚ“ęŌŚ¼«ŠŌ¹²¼Ū¼ü |
| B£®ŗĻ³ÉO4µÄ·“Ó¦æÉæ“×÷ŗĖ¾Ū±ä·“Ó¦£¬¼“²»ŹōÓŚ»Æѧ±ä»Æ |
| C£®O4ÓėO3”¢O2¶¼ŹĒŃõµÄĶ¬ĖŲŅģŠĪĢå |
| D£®O4½«Ą“æÉÓĆ×÷øüĒæÓŠĮ¦µÄ»š¼żĶĘ½ųµÄŃõ»Æ¼Į |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 Ӣ
Ӣ Ӣ
Ӣ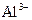 Ӣ
Ӣ Ӣ
”¢ µČĪåÖÖĄė×Ó°“°ė¾¶Óɓ󵽊”µÄĖ³ŠņÅÅĮŠ£ØÓĆĄė×Ó·ūŗűķŹ¾£©____________________”£
µČĪåÖÖĄė×Ó°“°ė¾¶Óɓ󵽊”µÄĖ³ŠņÅÅĮŠ£ØÓĆĄė×Ó·ūŗűķŹ¾£©____________________”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®3ÖÖ | B£®6ÖÖ | C£®9ÖÖ | D£®12ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 ²īŅģµÄŹĒC Ō×Ó½į¹¹
²īŅģµÄŹĒC Ō×Ó½į¹¹A£® | B£® | C£®1s22s22p3 | D£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¶ĢÖÜĘŚŌŖĖŲÖŠ£¬×īĶā²ćµē×ÓŹżŹĒĘäµē×Ó²ćŹżĮ½±¶µÄŌŖĖŲ¹²ÓŠ3ÖÖ |
| B£®µŚČżÖÜĘŚŌŖĖŲµÄĄė×Ó°ė¾¶“óŠ”±Č½Ļ£ŗCl->S2+>Na+>Mg2+>Al3+ |
| C£®ČÕ±¾ø£µŗŗĖµēÕ¾ŹĶ·Å³öµÄ·ÅÉäŠŌŗĖĖŲ131IÓė132I”¢133I»„ĪŖĶ¬Ī»ĖŲ |
| D£®ĻąĶ¬Ģõ¼žĻĀ£¬Ķعż²ā¶ØĶ¬ÅØ¶ČµÄNa2CO3ČÜŅŗŗĶNa2SO4ČÜŅŗµÄpH£¬æÉ±Č½ĻCŗĶSµÄ·Ē½šŹōŠŌĒæČõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ČōXŹĒŃõ£¬ŌņYX”Ŗ¶ØŹĒĄė×Ó»ÆŗĻĪļ |
| B£®ČōYŹĒŃõ£¬Ōņ·Ē½šŹōŠŌZ”µY”µX |
| C£®ČōXŹĒÄĘ£¬ŌņZµÄ×īøßÕż¼ŪŅ»¶ØĪŖżŹż |
| D£®ČōYŹĒÄĘ£¬ŌņX”¢Z²»æÉÄÜŹĒĶ¬Ņ»Ö÷×å |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com