
【题目】如图所示的装置中,M为金属活动性顺序表中位于氢之前的金属,N为石墨棒,下列关于此装置的叙述中不正确的是

A.N上有气体放出
B.M为负极,N为正极
C.是化学能转变为电能的装置
D.导线中有电流通过,电流方向是由M到N
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 新制的氯水在光照条件下颜色变浅
B. 合成氨工业中使用铁触媒作催化剂
C. 红棕色的NO2气体,加压后颜色先变深后变浅
D. 工业生产硫酸的过程中,通入过量的空气以提高二氧化硫的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,向20mL 0.1mol/L的醋酸溶液中不断滴加0.1mol/L的NaOH溶液,溶液的pH变化曲线如图所示,在滴定过程中,下列关于溶液中离子浓度大小关系的描述不正确的是
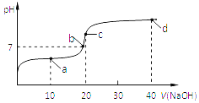
A. a点时:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-)
B. b点时:c(Na+) = c(CH3COO-)
C. c点时:c(OH-) =c(CH3COOH) + c(H+)
D. d点时:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素,它们的核电荷数均小于18,且原子序数逐渐增大。已知:A、C、F三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水。D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。请回答下列问题:
(1)写出D的元素符号_____________,E的最高价氧化物的水化物的分子式_____________。
(2)画出B元素的原子结构示意图_____________。
(3)若构成F元素的一种核素的中子数为18,写出该核素的表示符号_____________。
(4)A与C、C与F元素最高价氧化物的水化物反应的离子方程式依次为:_____________、_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】理论上讲,任何自发的氧化还原反应都可以设计成原电池。某同学利用“Cu+2Ag+=2Ag+Cu2+”反应设制一个化学电池,如图所示,已知该电池在外电路中,电流从a极流向b极。请回答下列问题:

(1)b极是电池的_____________极,材料是_____________,写出该电极的反应式_____________。
(2)a可以为_____________A、铜B、银C、铁D、石墨
(3)c溶液是_____________A、CuSO4溶液B、AgNO3溶液C、酒精溶液
(4)若该反应过程中有0.2mol电子发生转移,则生成Ag为_____________克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、是中学化学中常见的物质,它们之间的转化关系如图所示(部分产物已略去):

请回答下列问题:
(1)若X是强氧化性单质,则A不可能是_____(填序号)。
a.C b.N2 c.S d.Na e.Mg
(2)若B是能使品红试液褪色的无色气体,则B转化为C的化学方程式为:_____。
(3)若A、B、C三种化合物的水溶液均呈酸性,写出A和B反应的化学方程式:_____。C溶于水会生成D,D的浓溶液与铜加热时反应产生了1.12L气体(标况下),则被还原的D的物质的量是_____mol,转移的电子数是个_____。
(4)若X是金属单质,向B、C的溶液中分别滴加AgNO3溶液和稀硝酸均产生白色沉淀,则B的化学式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 15g甲基含有的电子数为10NA
B. 1mol2,2,3-三甲基丁烷含有非极性共价键总数为23 NA
C. 14g乙烯和环丙烷的混合物所含的原子总数为6NA
D. 在常温常压下,11.2L CH3Cl的质量小于25.25g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应2SO2+ O22SO3,当生成2 mol SO3时放出热量为Q,现将1 mol SO2和0.5 mol O2在相同条件下反应生成SO3放出的热量为Q1,则
A.Q1=![]() QB.Q1<
QB.Q1<![]() QC.2Q1>QD.无法判断
QC.2Q1>QD.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关Na2CO3和NaHCO3的叙述中正确的是
A. 向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1:2
B. 等质量的NaHCO3和Na2CO3分別与足量盐酸反应,在同温同压下。生成的CO2体积相同
C. 物质的量浓度相同时,Na2CO3溶液的pH小于NaHCO3溶液
D. 向Na2CO3饱和溶液中通入CO2有NaHCO3结晶析出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com