
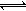 N2(g)+CO2(g) ��H.ij�о�С����ij�ܱ������м���һ�����Ļ���̿��NO�����£�T1�棩�����·�Ӧ����Ӧ���е���ͬʱ�̲�ø����ʵ�Ũ�����£�
N2(g)+CO2(g) ��H.ij�о�С����ij�ܱ������м���һ�����Ļ���̿��NO�����£�T1�棩�����·�Ӧ����Ӧ���е���ͬʱ�̲�ø����ʵ�Ũ�����£�| Ũ��/mol?L-1 ʱ��/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |

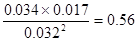 ��
��

 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
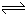 xC(g)+2D(g) ����H>0����5min���֪D��Ũ��Ϊ0.5mol/L��
xC(g)+2D(g) ����H>0����5min���֪D��Ũ��Ϊ0.5mol/L���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A������ˮ�д�������ƽ�⣺Br2+H2O  HBr+HBrO������NaOH��Һ����ɫ��dz HBr+HBrO������NaOH��Һ����ɫ��dz |
B����2HI H2��I2(g)ƽ����ϵ����ѹǿʹ��ɫ���� H2��I2(g)ƽ����ϵ����ѹǿʹ��ɫ���� |
C����ӦCO��NO2 CO2+NO ��H��0�����¶�ʹƽ�����淽���ƶ� CO2+NO ��H��0�����¶�ʹƽ�����淽���ƶ� |
D���ϳɰ���Ӧ��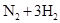  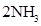 ����H��0 Ϊʹ���IJ�����ߣ�������Ӧ��ȡ���¸�ѹ�Ĵ�ʩ ����H��0 Ϊʹ���IJ�����ߣ�������Ӧ��ȡ���¸�ѹ�Ĵ�ʩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
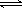 2NH3(g) ������˵���У�������һ��Ӧ�Ѿ��ﵽ��ѧƽ��״̬���ǣ� ��
2NH3(g) ������˵���У�������һ��Ӧ�Ѿ��ﵽ��ѧƽ��״̬���ǣ� �� | A��N2��H2��NH3���ܱ������й��� |
| B��N2��H2��NH3��Ũ����� |
| C��N2��H2��NH3��Ũ�Ȳ��ٱ仯 |
| D����Ӧֹͣ�������淴Ӧ���ʶ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Ӧ��ʼʱ�����ʣ���<�� |
| B����Ӧ�����ʱ�䣺��<�� |
| C����Ӧ��ʼʱ��������ʵ���Ũ�ȣ���<�� |
| D����Ӧ����ʱ��pHֵ����<�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��RCl>RI> R2CrO4 | B��RCl> R2CrO4>RI |
| C��R2CrO4>RCl>RI | D��R2CrO4>RI>RCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2z�ﵽƽ��ʱ�������ǵ����ʵ�������n(x)+n(y)=n(z)����y��ת����Ϊ( )
2z�ﵽƽ��ʱ�������ǵ����ʵ�������n(x)+n(y)=n(z)����y��ת����Ϊ( )| A����a+b��/5��100% | B��2��a+b��/5b��100% |
| C��2��a+b��/5��100% | D����a+b��/5a��100% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NO(g)+O2(g)���ﵽƽ��״̬�ı�־��( )
2NO(g)+O2(g)���ﵽƽ��״̬�ı�־��( )| A��NO2������������NO������������� |
| B��������ѹǿ����ʱ��仯���仯 |
| C��NO��O2����������֮��Ϊ2��1 |
| D�������и�������ʵ�Ũ�ȱ�Ϊ[NO2]��[NO]��[O2]��2:2:1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)��zD(g)����2 s��A��ת����Ϊ50%�����v(D)��0.25 mol��L��1��s��1�������ƶ���ȷ����(����)
2C(g)��zD(g)����2 s��A��ת����Ϊ50%�����v(D)��0.25 mol��L��1��s��1�������ƶ���ȷ����(����)�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com