
某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。

请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是________,其中发生反应的化学方程式为________________________________________________________________________。
(2)实验过程中,装置B、C中发生的现象分别是____________________________________、______________________________________;
这些现象分别说明SO2具有的性质是________________和________________;装置B中发生反应的离子方程式为______________________________________________________
________________________________________________________________________。
(3)装置D的目的是探究SO2与品红反应的可逆性,请写出实验操作及现象________________________________________________________________________
________________________________________________________________________。
(4)尾气可采用________溶液吸收。
答案 (1)蒸馏烧瓶 Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O
(2)溶液由紫红色变为无色 无色溶液中出现黄色浑浊 还原性 氧化性 5SO2+2MnO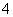 +2H2O===2Mn2++5SO
+2H2O===2Mn2++5SO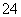 +4H+
+4H+
(3)品红溶液褪色后,关闭分液漏斗的活塞,点燃酒精灯加热,溶液恢复为红色
(4)NaOH(答案合理即可)
解析 (1)装置A中盛放亚硫酸钠的仪器带有支管,因此是蒸馏烧瓶(注意与圆底烧瓶的区别)。(2)由于SO2中S的价态处于中间价态,故既有氧化性又有还原性,所以通过酸性KMnO4溶液时被氧化,酸性KMnO4溶液被还原,溶液颜色由紫红色变为无色;通过Na2S溶液时,SO2体现氧化性,发生归中反应,生成单质硫,可看到无色溶液中出现黄色浑浊。(3)SO2漂白品红是可逆的,加热褪色后的溶液又会恢复为红色。(4)吸收酸性气体SO2应使用碱性溶液,如NaOH溶液。


科目:高中化学 来源: 题型:
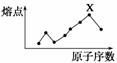
原子序数小于18的八种连号元素,它们的单质熔点随原子序数增大而变化的趋势如图所示,图中X元素应属于( )
A.ⅢA族 B.ⅣA族
C.ⅤA族 D.ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液能够区别SO2和CO2气体的是( )
①澄清的石灰水 ②H2S溶液 ③酸性KMnO4溶液
④氯水 ⑤品红溶液
A.①②③ B.②③④
C.除①以外 D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
以下每个选项中的两组物质都能反应,且能放出同一种气体的是( )
A.铜与稀硫酸,铜与浓硫酸
B.铁与稀硫酸,铁与浓硫酸
C.硫化钠与稀硫酸,亚硫酸钠与稀硫酸
D.硫化钠与稀硫酸,硫化钠与稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同( )
(2014·大纲全国卷,8A)
(2)用KOH溶液鉴别SO3(g)和SO2( )
(2014·重庆理综,2A)
(3)二氧化硫可广泛用于食品的增白( )
(2013·四川理综,1A)
(4)Na2S2O3溶液中加入稀硫酸的离子方程式:2S2O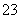 +4H+===SO
+4H+===SO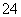 +3S↓+2H2O( )
+3S↓+2H2O( )
(2013·四川理综,3D)
查看答案和解析>>
科目:高中化学 来源: 题型:
具有广泛用途的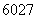 Co放射源首次实现了国内批量生产。另外,钴还有多种原子,如
Co放射源首次实现了国内批量生产。另外,钴还有多种原子,如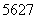 Co、
Co、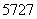 Co、
Co、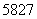 Co和
Co和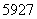 Co。下列关于钴原子的说法正确的是( )
Co。下列关于钴原子的说法正确的是( )
A.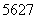 Co、
Co、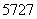 Co、
Co、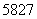 Co、
Co、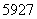 Co和
Co和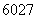 Co是摩尔质量不同的五种同素异形体
Co是摩尔质量不同的五种同素异形体
B.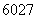 Co放射源可以用来治疗癌症,其中子数与电子数之差等于6
Co放射源可以用来治疗癌症,其中子数与电子数之差等于6
C.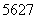 Co、
Co、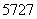 Co、
Co、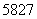 Co、
Co、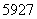 Co和
Co和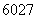 Co互为同位素,物理性质不同,化学性质几乎完全相同
Co互为同位素,物理性质不同,化学性质几乎完全相同
D.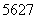 Co、
Co、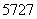 Co、
Co、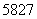 Co、
Co、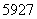 Co和
Co和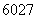 Co互为同分异构体
Co互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
相同质量的铜片分别与体积相同且过量的浓硝酸、稀硝酸反应,二者比较相等的是( )
A.反应中氧化剂得到电子总数
B.铜片消耗完所需时间
C.反应后溶液中铜离子浓度(反应后溶液体积不变)
D.反应生成气体的体积(同温、同压)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com