
| A. | 0.1(y-2x)mol/L | B. | 10(2x-y)mol/L | C. | 10(y-x)mol/L | D. | 10(y-2x)mol/L |
分析 混合溶液分成三等份,每份溶液浓度相同,一份加入含x mol 硫酸钾的溶液,发生反应Ba2++SO42-=BaSO4↓,恰好使钡离子完全沉淀,可知该份中n(Ba2+)=(Na2SO4);
另一份加入含ymol硝酸银的溶液,发生反应Ag++Cl-=AgCl↓,恰好使氯离子完全沉淀,则n(Cl-)=n(Ag+),
再利用电荷守恒可知每份中2n(Ba2+)+n(Na+)=n(Cl-),据此计算每份中n(Na+),根据c=$\frac{n}{V}$计算钠离子浓度.
解答 解:混合溶液分成三等份,每份溶液浓度相同,一份加入含axmol 硫酸钠的溶液,发生反应Ba2++SO42-=BaSO4↓,恰好使钡离子完全沉淀,可知该份中n(Ba2+)=(Na2SO4)=xmol;
另一份加入含ymol 硝酸银的溶液,发生反应Ag++Cl-=AgCl↓,恰好使氯离子完全沉淀,则n(Cl-)=n(Ag+)=ymol,
根据电荷守恒可知每份中2n(Ba2+)+n(Na+)=n(Cl-),每份溶液中n(Na+)=ymol-2xmol=(y-2x)mol,
故钠离子浓度=$\frac{y-2x}{0.1}$mol/L=10(y-2x)mol/L,
故选D.
点评 本题考查物质的量浓度的有关计算,为高频考点,侧重考查学生分析计算能力,明确各个物理量之间的关系是解本题关键,注意每一份体积是100mL而不是300mL,为易错点.


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L氧气反应时特移电子数为2NA | |
| B. | 1molCnH2n+2(n≥2)中含有的C-C键数为(n-1)NA | |
| C. | 0.1mol24Mg32S晶体中所含中子总数为28NA | |
| D. | 标准状况下,11.2LSO3所含的分子数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
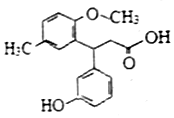
| A. | 所有碳原子可以共平面 | B. | 分子中有1个手性碳原子 | ||
| C. | 能与Na2CO3溶液反应 | D. | 能发生加成、取代、消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑧ | B. | ①⑥ | C. | ②④ | D. | ③⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
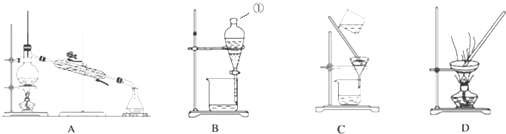
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com