
| A. | 氧化性强弱顺序为XO42->Z2>R2>M3+ | |
| B. | Z2在③中发生氧化反应 | |
| C. | R元素在反应②中被氧化,在③中被还原 | |
| D. | 常温下反应不可进行2M2++Z2═2M3++2Z- |
分析 ①H++Z-+XO42-→X2++Z2+H2O,反应中XO4-是氧化剂,Z2是氧化产物,氧化性:XO4->Z2;
②2M2++R2═2M3++2R-,反应中R2是氧化剂,M3+是氧化产物,氧化性:R2>M3+;
③2R-+Z2═R2+2Z-,反应中Z2是氧化剂,R2是氧化产物,氧化性:Z2>R2;
所以氧化性强弱关系为:XO4->Z2>R2>M3+,以此解答该题.
解答 解:①H++Z-+XO42-→X2++Z2+H2O,反应中XO4-是氧化剂,Z2是氧化产物,氧化性:XO4->Z2;
②2M2++R2═2M3++2R-,反应中R2是氧化剂,M3+是氧化产物,氧化性:R2>M3+;
③2R-+Z2═R2+2Z-,反应中Z2是氧化剂,R2是氧化产物,氧化性:Z2>R2;
所以氧化性强弱关系为:XO4->Z2>R2>M3+,
A.所以氧化性强弱关系为:XO4->Z2>R2>M3+,故A正确;
B.③2R-+Z2═R2+2Z-,反应中Z2是氧化剂,发生还原反应,故B错误;
C.R元素在反应②中做氧化剂,被还原,在③中做还原剂,被氧化,故C错误;
D.反应2M2++Z2═2M3++2Z-中,Z2是氧化剂,M3+是氧化产物,氧化性Z2>M3+,符合题意,故D错误;
故选:A.
点评 本题考查了氧化性、还原性强弱比较,明确氧化还原反应强弱规律,准确判断氧化剂、氧化产物、还原剂、还原产物是解题关键,题目难度不大.


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:填空题
| 物质 | CH3OH | CH3OCH3 | H2O |
| c/mol•L-1 | 0.44 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
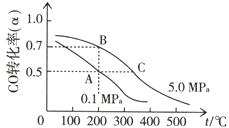 “洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ•m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.
“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了热值高达122500~16000kJ•m-3的煤炭气,其主要成分是CO和H2.CO和H2可作为能源和化工原料,应用十分广泛.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 提高风能、太阳能等可再生清洁能源的使用比例 | |
| B. | 推广CO2再利用技术,将其合成有价值的化学品 | |
| C. | 利用工业废水灌溉农作物,提高水资源的利用率 | |
| D. | 研发煤炭的洁净、高效利用技术,保护生态环境 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石蕊,由蓝变红 | B. | 酚酞,红色褪去 | C. | 甲基橙,由黄变橙 | D. | 甲基橙,由橙变黄 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入22.4LSO2参加反应时,有2 NA个电子发生转移 | |
| B. | 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 | |
| C. | 滴加KI溶液时,KI被氧化,CuI是氧化产物 | |
| D. | 通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2通入CaCl2溶液中 | B. | NO2通入FeSO4溶液中 | ||
| C. | NH3通入A1C13溶液中 | D. | SO2通入Ba(NO3)2溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 100 |
| KW/10-14 | 0.114 | 0.292 | 0.681 | 1.00 | 2.92 | 5.47 | 55.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com