
| A. | 100 mL 1 mol/L的盐酸中含HCl分子数为0.1NA | |
| B. | 7.8 g Na2O2和Na2S的混合物中阴离子数目为0.2NA | |
| C. | 标准状况下,2.24 L SO3中含有氧原子数目为0.3NA | |
| D. | 2 g D216O中含中子、质子、电子数目均为NA |
分析 A、HCl溶于水后能完全电离;
B、Na2O2和Na2S的摩尔质量均为78g/mol,且均由2个钠离子和1个阴离子构成;
C、标况下三氧化硫为固体;
D、求出2 g D216O的物质的量,然后根据重水中含10个电子、10个质子和10个中子来分析.
解答 解:A、HCl溶于水后能完全电离,故盐酸溶液中无氯化氢分子,故A错误;
B、Na2O2和Na2S的摩尔质量均为78g/mol,故7.8g混合物的物质的量为0.1mol,且两者均由2个钠离子和1个阴离子构成,故0.1mol混合物中含0.1NA个阴离子,故B错误;
C、标况下三氧化硫为固体,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、2 g D216O的物质的量为0.1mol,而重水中含10个电子、10个质子和10个中子,故0.1mol重水中含电子、质子和中子个数均为NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:推断题
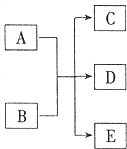 一定条件,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.
一定条件,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小顺序:D>C>B>A | |
| B. | y、p 中均只含有离子键 | |
| C. | B、D两元素最高价氧化物对应水化物分别为强酸、强碱 | |
| D. | p能抑制水的电离而q能促进水的电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 项 目 | 每100克(g) | 营养素参考值% |
| 能 量 | 1500kJ | 18% |
| 蛋 白 质 | 0g | 0% |
| 脂 肪 | 2.0g | 3% |
| 碳水化合物 | 72g | 24% |
| 钠 | 30mg | 2% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①=②=③=④ | B. | ③>②>①>④ | C. | ④>②>①>③ | D. | ③>①>②>④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 探究上述四种酸的氧化性相对强弱及其与铜反应的还原产物的性质:
探究上述四种酸的氧化性相对强弱及其与铜反应的还原产物的性质:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
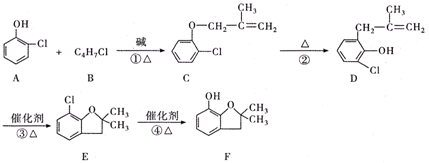
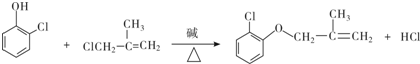 (有机物用结构简式表示,下同).
(有机物用结构简式表示,下同).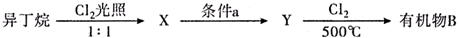
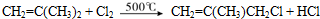 ;
;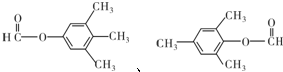
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com