
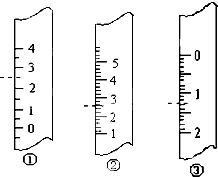
 如图分别是温度计、量筒、滴定管的一部分,则:量筒应该是
如图分别是温度计、量筒、滴定管的一部分,则:量筒应该是 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
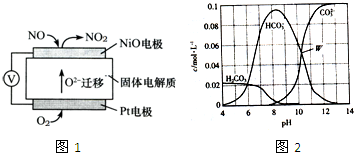 根据化学反应原理,回答下列问题:
根据化学反应原理,回答下列问题:c(HC
| ||
c(C
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N4属于一种新型的化合物 |
| B、N4和N2互为同位素 |
| C、N4与N2互为同素异形体 |
| D、1molN4气体转变为N2将吸收882kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硅是一种亲氧元素,在自然界中它总是与氧相互化合的 |
| B、氯气是一种有毒的黄绿色气体,但可用于自来水的杀菌消毒 |
| C、为了防止食品受潮及富脂食品氧化变质,常在包装袋中放入硅胶和硫酸亚铁 |
| D、白色污染、绿色食品中的“白”、“绿”均指相关物质的颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
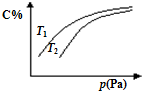 在密闭容器中,对于可逆反应A+3B?2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )
在密闭容器中,对于可逆反应A+3B?2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )| A、若正反应方向△H<0,则T1>T2 |
| B、压强增大时,混合气体的密度减小 |
| C、A一定为气体 |
| D、B一定为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 稀HNO3 |
| HCl |
| O2/点燃 |
| H2O |
| KMnO4(s) |
| NaOH(aq) |
| HCl |
| △ |
| A、①② | B、①③ | C、②④ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①中X2+是还原产物 |
| B、还原性强弱的顺序为:Z->A2+ |
| C、氧化性强弱的顺序为:XO4->B2 |
| D、溶液中可发生:Z2+2A2+=2A3++2Z- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 按要求书写下列热化学方程式
按要求书写下列热化学方程式查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com